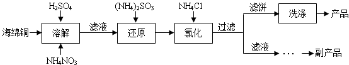
题目内容
14.在含有1mol Fe3+和1mol Al3+的混合溶液中,现按横坐标依次加入NaOH溶液、盐酸,再通CO2气体.纵坐标为混合沉淀物的物质的量.(1)请在图中画出沉淀量随反应变化的曲线:
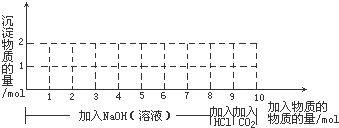
(2)写出通入CO2后的有关的离子方程式:CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-;CO2+CO32-+H2O=2HCO3-.
分析 (1)含1molFe3+和1molAl3+的混合溶液中,加6molNaOH两种离子完全转化为沉淀,再加1molNaOH时Al(OH)3完全溶解生成偏铝酸根离子,7~8mol时加NaOH不发生反应,8~9mol时加盐酸,发生酸碱中和,9~10mol通入CO2气体,偏铝酸根离子转化为Al(OH)3,碳酸根离子转化为碳酸氢根离子;
(2)通入CO2后,也就是9-10为偏铝酸根离子转化为Al(OH)3及碳酸根离子转化为碳酸氢根离子的反应.
解答 解:(1)含1molFe3+和1molAl3+的混合溶液中,加6molNaOH两种离子完全转化为沉淀,再加1molNaOH时Al(OH)3完全溶解生成偏铝酸根离子,7~8mol时加NaOH不发生反应,8~9mol时加盐酸,发生酸碱中和,9~10mol通入CO2气体,偏铝酸根离子转化为Al(OH)3,碳酸根离子转化为碳酸氢根离子,沉淀的物质的量随反应的变化曲线为 ,
,
故答案为: ;
;
(2)9-10为偏铝酸根离子转化为Al(OH)3及碳酸根离子转化为碳酸氢根离子的反应,发生的反应为CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-、CO2+CO32-+H2O=2HCO3-,
故答案为:CO2+2AlO2-+3H2O=2Al(OH)3↓+CO32-;CO2+CO32-+H2O=2HCO3-.
点评 本题考查离子反应方程式的书写,明确加入物质发生的化学反应及反应与图象的对应关系是解答本题的关键,并利用离子反应方程式的书写方法来解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.X、Y、Z均为短周期元素,其简单离子X+、Y3+、Z2-的核外电子层结构相同.下列说法不正确的是( )
| A. | 离子半径:X+>Y3+>Z2- | B. | 原子序数:Y>X>Z | ||
| C. | 电负性:Z>Y>X | D. | 单质的还原性:X>Y |
2.下列物质中不能用于萃取溴水中溴的是( )
| A. | 直馏汽油 | B. | 裂化汽油 | C. | 苯 | D. | 己烷 |
9.向一定量Fe3O4和Fe的混合物中加入50mL2mol•L-1H2SO4溶液,恰好使混合物完全溶解,放出448mL(标准状况下)的气体.向所得溶液中加入KSCN溶液,无红色出现.则用足量的CO在高温下与相同质量的此混合物充分反应,能得到铁的质量为( )
| A. | 2.8g | B. | 5.6g | C. | 11.2g | D. | 22.4g |
3.配制一定物质的量浓度的溶液时,下列操作会导致所配溶液浓度偏高的是( )
| A. | 定容时仰视容量瓶的刻度线 | |
| B. | 在用蒸馏水洗涤烧杯时,洗涤液未全部转移到容量瓶中 | |
| C. | 配制盐酸溶液用量筒量取浓盐酸时仰视刻度线 | |
| D. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 |
 .
.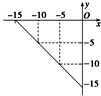 某温度下的溶液中,c (H+)=10x mol/L,c (OH-)=10y mol/L.
某温度下的溶液中,c (H+)=10x mol/L,c (OH-)=10y mol/L. 中带*的C原子.若同一个碳原子上连着2个碳碳双键(如C═C═C)时,分子极不稳定,不存在.某链烃C7H10的众多同分异构体中:
中带*的C原子.若同一个碳原子上连着2个碳碳双键(如C═C═C)时,分子极不稳定,不存在.某链烃C7H10的众多同分异构体中:
 、
、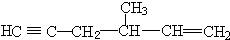 .
. 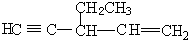 .
.