题目内容
下列装置中四块相同的Zn片,放置一段时间后腐蚀速率由慢到快的顺序是( )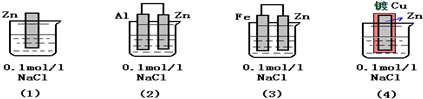

| A、(1)(3)(2)(4) |
| B、(4)(2)(1)(3) |
| C、(3)(2)(1)(4) |
| D、(4)(1)(2)(3) |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:电化学腐蚀较化学腐蚀快,金属得到保护时,腐蚀较慢,作原电池正极和电解池阴极的金属被保护,金属腐蚀快慢顺序是:电解池阳极>原电池负极>化学腐蚀>原电池正极>电解池阳极..
解答:
解:金属腐蚀快慢顺序是:电解池阳极>原电池负极>化学腐蚀>原电池正极>电解池阳极,
(1)中锌发生化学腐蚀,加快锌的腐蚀,(2)中锌作原电池的正极,被保护,(3)中锌作原电池的负极,被腐蚀,(4)Zn的外面镀铜,Zn被保护,所以腐蚀速率由慢到快的顺序是(4)(2)(1)(3).
故选B.
(1)中锌发生化学腐蚀,加快锌的腐蚀,(2)中锌作原电池的正极,被保护,(3)中锌作原电池的负极,被腐蚀,(4)Zn的外面镀铜,Zn被保护,所以腐蚀速率由慢到快的顺序是(4)(2)(1)(3).
故选B.
点评:本题考查不同条件下金属腐蚀的快慢,明确腐蚀快慢为:电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护腐蚀措施的腐蚀即可解答.

练习册系列答案
相关题目
由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20.下列说法中正确的是( )
| A、化合物中阳离子和阴离子的个数不一定相等 |
| B、化合物中一定只有离子键没有共价键 |
| C、所含元素一定不在同一周期也不在第一周期 |
| D、化合物中阳离子半径一定大于阴离子半径 |
在一定温度下,一恒容容器中发生反应2A2(g)+B2(g)?2AB(g),该反应达到平衡状态的标志是( )
| A、单位时间生成n mol的A2同时生成n mol的AB |
| B、容器内的总压强不随时间变化 |
| C、容器内的气体密度不随时间变化 |
| D、单位时间内生成n mol的A2同时生成n mol的B2 |
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应为Zn+2MnO2+H2O═Zn(OH)2+Mn2O3,下列说法错误的是( )
| A、电池工作时,锌失去电子 |
| B、电池正极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- |
| C、电池工作时,负极附近pH降低 |
| D、正极是水电离出的H+得到电子 |
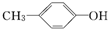 ;③
;③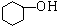 ;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦
;④CH3CH2Cl;⑤CCl4;⑥CH≡CH;⑦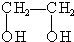 ; ⑧CH3CH2OH.
; ⑧CH3CH2OH.