题目内容
下列离子方程式正确的是( )
A.硫化钠水解 S2-+2H2O H2S+2OH- H2S+2OH- |
B.硫氢化钠的水解 HS-+H2O H3O++S2- H3O++S2- |
C.不断加热煮沸氯化铁溶液 Fe3++3H2O Fe(OH)3+3H+ Fe(OH)3+3H+ |
| D.硫酸铝溶液跟NaHCO3溶液反应 Al3++3HCO3-=Al(OH)3↓+3CO2↑ |
D
解析试题分析:A.多元弱酸根离子分步水解,硫化钠水解 S2-+H2O HS― +OH-, A错误;B.硫氢化钠的水解应为:HS-+H2O
HS― +OH-, A错误;B.硫氢化钠的水解应为:HS-+H2O H2S+OH―, HS-+H2O
H2S+OH―, HS-+H2O H3O++S2-是电离方程式,B错误;C.不断加热煮沸氯化铁溶液,Fe3+ 会水解完全,生成沉淀,Fe3++3H2O
H3O++S2-是电离方程式,B错误;C.不断加热煮沸氯化铁溶液,Fe3+ 会水解完全,生成沉淀,Fe3++3H2O Fe(OH)3↓+3H+,C错误;D.硫酸铝溶液跟NaHCO3溶液反应 Al3++3HCO3-=Al(OH)3↓+3CO2↑,双水解,D正确;
Fe(OH)3↓+3H+,C错误;D.硫酸铝溶液跟NaHCO3溶液反应 Al3++3HCO3-=Al(OH)3↓+3CO2↑,双水解,D正确;
选D。
考点:盐类水解的原理;离子方程式的书写

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
则下列有关说法正确的是
A.等物质的量浓度的各溶液pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.a mol·L-1 HCN溶液与a mol·L-1 NaOH溶液等体积混合后,所得溶液显碱性(pH>7),则c (OH-)>c(H+)、c(Na+)>c(CN-)
C.冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+) = c(OH-)+c(HCO3-)+c(CO32-)
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是(提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡常数Ksp = c(Ba2+)·c(SO42-),称为溶度积常数。)
Ba2+(aq)+SO42-(aq)的平衡常数Ksp = c(Ba2+)·c(SO42-),称为溶度积常数。)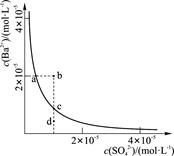
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.d点无BaSO4沉淀生成 |
| C.通过蒸发可以使溶液由d点变到c点 |
| D.a点对应的Ksp大于c点对应的Ksp |
用0.10 mol/L 的盐酸滴定0.10 mol/L 的氨水,滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl ),c(OH ),c(OH )>c(H )>c(H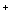 ) ) | B.c(NH4+) = c(Cl ),c(OH ),c(OH ) = c(H ) = c(H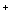 ) ) |
C.c(Cl )>c(NH4+),c(OH )>c(NH4+),c(OH )>c(H )>c(H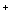 ) ) | D.c(Cl )>c(NH4+),c(H )>c(NH4+),c(H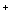 )>c(OH )>c(OH ) ) |
下列物质加入水中,对水的电离能产生促进作用的是
| A.NH4Cl | B.NaOH | C.NaCl | D.H2SO4 |
常温下amo1/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判断一定错误的是
| A.c(OH一)>c(H+)时,a=b | B.c(K+)>c(CH3COO—)时,a>b |
| C.c(OH一)=c(H+)时,a>b | D.c(K+)<c(CH3COO—)时,a<b |
一定温度下的难溶电解质在水溶液中达到溶解平衡时。已知下表数据
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀时的PH值 | ≥9.6 | ≥6.4 | 3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是
A.向该溶液中加少量铁粉不能观察到红色固体析出
B.该溶液中c(SO42-):[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5:4
C.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
D.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
下列叙述正确的是:( )
| A.95℃时纯水的pH<7,说明加热可导致水呈酸性 |
| B.将pH=3的CH3COOH溶液加水稀释10倍后pH=4 |
| C.0.2 mol/L的盐酸1L加水到2L后,溶液的pH=1 |
| D.NaHCO3溶液水解反应的方程式: HCO3-+ H2O = H3O++ CO32- |
某温度下,
 分别在溶液中达到沉淀溶解平衡后,改变溶液
分别在溶液中达到沉淀溶解平衡后,改变溶液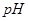 ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
A. |
B.加适量 固体可使溶液由 固体可使溶液由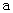 点变到 点变到 点 点 |
C.  两点代表的溶液中 两点代表的溶液中 与 与 乘积相等 乘积相等 |
D. 、 、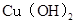 分别在 分别在 、 、 两点代表的溶液中达到饱和 两点代表的溶液中达到饱和 |