题目内容
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下图所示,其中Q是无机非金属材料的主角。下列判断正确的是
| | | R | | |
| T | Q | | W | G |
A.离子半径:T< W< G
B.最简单气态氢化物的热稳定性:Q < R
C.最高价氧化物对应水化物的酸性:Q >W>G
D.T和G组成的化合物甲溶于水,其水溶液呈中性
B
解析试题分析:Q是无机非金属材料的主角,判定Q是硅元素,所以R、T、W、G分别是氮、铝、硫、氯元素。
A、W、G的离子的核外电子排布相同,核电荷数越多,半径越小,所以W>G,T的离子比W、G的离子少一个电子层,半径最小,错误;B、R的非金属性强于Q,所以最简单气态氢化物的热稳定性:Q < R,正确;C、Q、W、G的非金属性依次增强,所以最高价氧化物对应水化物的酸性依次增强,错误;D、T和G组成的化合物甲氯化铝属于强酸弱碱盐,溶于水后溶液呈酸性,错误,答案选B。
考点:考查元素对判断及元素周期律对应用

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
以下表示氦原子结构的化学用语中,对电子运动状态描述最详细的是( )
| A.He : | B.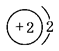 | C.1s2 | D.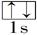 |
短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等。下列说法不正确的是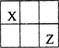
| A.原子半径:Y>Z>W |
| B.一定条件下,Y可置换出X |
| C.气态氢化物稳定性:Z>W |
| D.熔点YW2>XW4 |
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重
元素,该元素原子核内中子数与核外电子数之差是( )
| A.57 | B.47 | C.61 | D.293 |
几种短周期元素的原子半径及主要化合价如下表: 
下列叙述正确的是 ( )
| A.X、Y元素的金属性 X<Y |
| B.一定条件下,Z单质与W的常见单质直接生成ZW2 |
| C.Y的最高价氧化物对应的水化物能溶于氨水 |
| D.Z的气态氢化物与其最高价氧化物对应的水化物可以反应 |
下列有关元素的性质及其递变规律正确的是
| A.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
| B.第二周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,水解程度越大 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
某元素X最高价含氧酸的分子量为98,且X的氢化物的分子式不是H2X,则下列说法正确的是( )
| A.X的最高化合价为+4 |
| B.X是第二周期VA族元素 |
| C.X是第二周VIA族元素 |
| D.X的最高价含氧酸的分子式可表示为H3XO4 |
根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
A.最高价氧化物对应水化物的碱性A>C
B.氢化物的沸点H2D>H2E
C.单质与稀盐酸反应的速率A<B
D.C2+与A+的核外电子数相等