题目内容
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、22.4L甲烷中含有C-H键的数目为4NA |
| B、46g NO2和N2O4的混合气体中含有原子总数为3NA |
| C、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| D、Na2O2与足量H2O反应,共生成0.1mol O2,转移电子的数目为0.4NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉在标准状况下,不能使用标况下的气体摩尔体积计算甲烷的物质的量;
B.NO2和N2O4的最简式为NO2,根据最简式计算出混合物中含有的原子的物质的量及数目;
C.缺少氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目;
D.过氧化钠中氧元素的化合价为-1价,生成0.1mol氧气转移了0.2mol电子.
B.NO2和N2O4的最简式为NO2,根据最简式计算出混合物中含有的原子的物质的量及数目;
C.缺少氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目;
D.过氧化钠中氧元素的化合价为-1价,生成0.1mol氧气转移了0.2mol电子.
解答:
解:A.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L甲烷的物质的量,故A错误;
B.46gNO2和N2O4的混合物中含有1mol最简式NO2,含有3mol原子,含有原子总数为3NA,故B正确;
C.没有告诉氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目,故C错误;
D.过氧化钠与水反应生成0.1mol氧气,转移了0.2mol电子,转移电子的数目为0.2NA,故D错误;
故选B.
B.46gNO2和N2O4的混合物中含有1mol最简式NO2,含有3mol原子,含有原子总数为3NA,故B正确;
C.没有告诉氢氧化钠溶液的体积,无法计算溶液中氢氧根离子的数目,故C错误;
D.过氧化钠与水反应生成0.1mol氧气,转移了0.2mol电子,转移电子的数目为0.2NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件,选项D为易错点,注意过氧化钠中氧元素的化合价为-1价.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
下列反应属于氮的固定的是( )
| A、Cl2将NH3氧化成N2 |
| B、NH3和HCl生成NH4Cl固体 |
| C、豆科植物将N2转化为NH4+ |
| D、空气中的氮氧化物转化成酸雨 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Fe2+、Al3+和Na+.某同学为了确认其成分,取部分试液,设计并完成了如下实验:
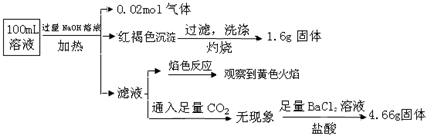
由此可知原溶液中( )

由此可知原溶液中( )
| A、原溶液中c(Fe3+)=0.2mol?L-1 |
| B、溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2mol?L-1 |
| C、SO42-、NH4+、Na+一定存在,CO32-、Al3+一定不存在 |
| D、要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入适量氯水,无现象,再加KSCN溶液,溶液成血红色,则含有Fe2+ |
下列实验能获得成功的是( )
| A、在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯 |
| B、用溴水可鉴别苯、CCl4、苯乙烯 |
| C、鉴定溴乙烷中存在溴元素的实验操作是先加入NaOH溶液,加热后再加入AgNO3溶液 |
| D、配制银氨溶液时,将硝酸银溶液逐滴加入到稀氨水中 |
在中和热的测定实验中,使用下列用品不是为了减少实验误差的是( )
| A、碎泡沫塑料 |
| B、环形玻璃搅拌棒 |
| C、底部垫纸条 |
| D、两个量筒 |
下列各组物质中,能用高锰酸钾酸性溶液鉴别的是( )
| A、乙烯、乙炔 |
| B、苯、正己烷 |
| C、1-己烯、二甲苯 |
| D、1-己炔、苯 |
根据氢原子和氯原子的核外电子排布,对Cl2和HCl分子中形成的共价键描述正确的( )
| A、两者都为s-sσ键 |
| B、两者都为p-pσ键 |
| C、前者为p-pσ键,后者为s-pσ键 |
| D、前者为s-sσ键,后者为s-pσ键 |
食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是( )
| A、炒菜时放入食盐并不破坏NaCl中的化学键 |
B、HCl的电子式是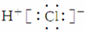 |
| C、NaCl熔化时破坏共价键 |
| D、HCl属于共价化合物 |