题目内容
【题目】31.04gFe3O4、Fe2O3、FeO组成的固体混合物,用180 mL6.0 mol·L-1盐酸能恰好将之完全溶解。若将此固体混合物用CO完全还原,则生成的铁的物质的量为
A.0.2molB.0.3molC.0.4molD.0.5mol
【答案】C
【解析】
Fe3O4、Fe2O3、FeO组成的固体混合物用CO还原,CO夺取混合物中的氧,生成Fe的质量=混合物总质量-减去混合物中氧元素质量,进而计算Fe的物质的量。而混合物用盐酸能恰好将之完全溶解,混合物中氧与氯化氢中的氢结合生成水,由O原子、H原子守恒可知n(O)=n(H2O)=![]() n(HCl),可得混合物中氧元素质量。
n(HCl),可得混合物中氧元素质量。
混合物用盐酸能恰好将之完全溶解,混合物中氧与氯化氢中的氢结合生成水,由O原子、H原子守恒可知n(O)=n(H2O)= ![]() n(HCl)=
n(HCl)=![]() ×0.18L×6.0mol/L=0.54mol,故生成Fe的质量=31.04g-0.54mol×16g/mol=22.4g,故n(Fe)=
×0.18L×6.0mol/L=0.54mol,故生成Fe的质量=31.04g-0.54mol×16g/mol=22.4g,故n(Fe)=![]() =0.4mol;故选:C。
=0.4mol;故选:C。

【题目】(14分)某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4 ·4H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
① | 4 | B= | 10 | 30 |
② | 5 | 60 | 10 | d= |
③ | a= | 60 | c= | 20 |
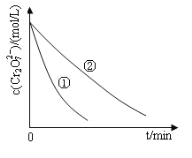
测得实验①和②溶液中的Cr2O72-浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化为 (填化学式);
(3)实验①和②的结果表明_______________________________;
(4)该课题组对铁明矾[Al2Fe(SO4)4 ·4H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用;假设二: ;假设三: ;……
(5)请你设计实验验证上述假设一,完成下表中内容。(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。(溶液中Cr2O72-的浓度可用仪器测定)
实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
取_______________________________代替实验①中的铁明矾,控制其他反应条件与实验①相同,进行对比实验 | 反应进行相同时间后, 若溶液中的Cr2O72-浓度____________________________则假设一成立; 若溶液中的Cr2O72-浓度____________________________则假设一不成立; |
(6)铁明矾长期存放,其中的亚铁离子可能会变质。为测定铁明矾中亚铁离子的质量分数。取5.6g铁明矾晶体,将其配制为100ml的溶液,取出20ml置于锥形瓶中。用0.01mol/L的标准KMnO4溶液进行滴定(还原产物为Mn2+),平行做4组实验,得出如下表数值。
组数 | 1 | 2 | 3 | 4 |
消耗V(KMnO4)/ml | 20.04 | 20.00 | 18.90 | 19.96 |
请计算铁明矾中亚铁离子的质量分数: 。若滴定结束后读数时仰视,测定结果 (填“偏大”“不影响”或“偏小”)