题目内容
【题目】已知化学方程式:![]() 。在该反应中,破坏1mol EG中的化学键需吸收能量Q1,破坏1mol JL中的化学键需吸收能量Q2,形成1mol EL中的化学键需放出能量Q3,形成1mol JG中的化学键需放出能量Q4若该反应放出能量,则下列关系式一定正确的是( )
。在该反应中,破坏1mol EG中的化学键需吸收能量Q1,破坏1mol JL中的化学键需吸收能量Q2,形成1mol EL中的化学键需放出能量Q3,形成1mol JG中的化学键需放出能量Q4若该反应放出能量,则下列关系式一定正确的是( )
A.Q1+ Q2> Q3+ Q4B.Q1< Q3+ Q4C.Q2< Q3D.Q2< Q4
【答案】B
【解析】
由化学方程式![]() 可知,该反应为复分解反应,放出能量。
可知,该反应为复分解反应,放出能量。
A.由化学方程式![]() 可知,该反应放出能量,则破坏化学键吸收的能量小于形成化学键放出的能量,即Q1+Q2<Q3+Q4,故A错误;
可知,该反应放出能量,则破坏化学键吸收的能量小于形成化学键放出的能量,即Q1+Q2<Q3+Q4,故A错误;
B.由于Q1+Q2<Q3+Q4,故Q1<Q3+Q4,故B正确;
C.对于有多种反应物和生成物参与的反应,无法判断一种反应物的能量与一种生成物的能量的相对大小,故C错误;
D.对于有多种反应物和生成物参与的反应,无法判断一种反应物的能量与一种生成物的能量的相对大小,故D错误;
故答案选B。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】二甲醚(CH3OCH3)是一种应用前景广阔的清洁燃科,以CO和氢气为原料生产二甲醚主要发生以下三个反应:
编号 | 热化学方程式 | 化学平衡常数 |
① | CO(g)+2H2(g) | K1 |
② | 2CH3OH(g) | K2 |
③ | CO(g)+H2O(g) | K3 |
回答下列问题:
工艺中反应①和反应②分别在不同的反应器中进行,无反应③发生。该工艺中反应③的发生提高了CH3OCH3的产率,原因是___。
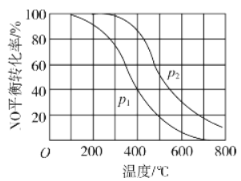
【题目】已知反应O2(g)+2Cl2(g) ![]() 2Cl2O(g) △H>0,在三个恒温、恒容的密闭容器中分别充人lmolO2与2molCl2,测得平衡时O2的转化率如下表.下列说法正确的是( )
2Cl2O(g) △H>0,在三个恒温、恒容的密闭容器中分别充人lmolO2与2molCl2,测得平衡时O2的转化率如下表.下列说法正确的是( )
容器编号 | 温度(℃) | 容器体积/L | 平衡时O2转化率 | 平衡时压强(Pa) |
① | 200 | V1 | 50% | P1 |
② | 200 | V2 | 70% | P2 |
③ | 350 | V3 | 50% | P3 |
A. 反应速率:③>①>②
B. 平衡时压强:P1>P2
C. 容器体积:V1<V3
D. 若实验②中O2和Cl2用量均加倍,则平衡时O2的转化率小于70%