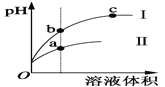
题目内容
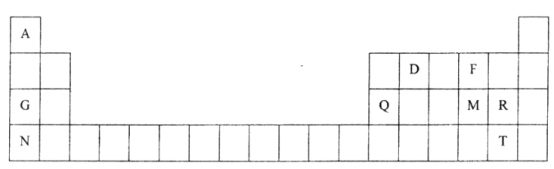
【题目】元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题。
(1)以上9种元素中金属性最强的元素是_______(填元素符号)。
(2)元素的非金属性:M______R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是_____________。
(4)F、G两元素形成的淡黄色固体物质的电子式为_____________。
(5)表中M、R、N元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_____________(用离子符号表示)。
【答案】K<HClO4![]() S2->Cl->K+
S2->Cl->K+
【解析】
由元素在周期表中的位置可知,A为H,D为C,F为O,G为Na,Q为Al,M为S,R为Cl,N为K,T为Br,然后结合元素化合物知识及元素周期律、化学用语等来解答.
(1)上述元素中金属性最强的为K元素;(2)同周期从左向右非金属性增强,则非金属性M<R;(3)R为Cl,最高价为+7价,则R的最高价氧化物对应水化物的化学式是HClO4;(4)F、G两元素形成的淡黄色固体物质的电子式为![]() ;(5)表中M、R、N元素,与Ar具有相同电子层结构的简单离子,原子序数大的离子半径小,则离子半径为S2->Cl->K+。
;(5)表中M、R、N元素,与Ar具有相同电子层结构的简单离子,原子序数大的离子半径小,则离子半径为S2->Cl->K+。

 名校课堂系列答案
名校课堂系列答案【题目】某小组在实验室使用软锰矿(主要成分为MnO2)和浓盐酸通过加热制备氧气,并对氯气的性质进行探究。
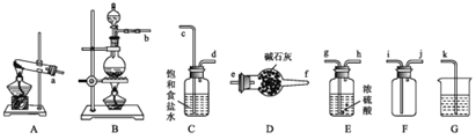
(1)写出实验室制氯气的化学方程式________。欲制取并收集一瓶干燥的氯气,则“制取→收集”的实验装置连接顺序为:____→c→d→_____→i→j→k
(2)装置C中饱和食盐水的作用是______________。
(3)该小组同学对氯气性质进行如下探究:
实验步骤 | 实验结论 |
①将氯气通入到NaCl溶液中,再加入1mL CCl4振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序: 氯、溴、碘 |
②将氯气通入到KBr溶液中,再加入1mL CCl4振荡,静置,观察四氯化碳层颜色 | |
③将氯气通入到KI溶液中,再加入1mL CCl4振荡,静置,观察四氧化碳层颜色 |
该小组的实验设计缺陷是___________,改进的办法是________________。
(4)常温下,高锰酸钾固体和浓盐酸反应也可制得氯气,该反应的离子方程式为______________。
(5)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的质量之比为______________。