题目内容
某元素X,其原子的电子层数为(n-1),最外层电子数为(2n-1).下列有关元素X的说法中正确的是( )
①元素X 可能是金属元素 ②元素X的气态氢化物一定极易溶于水 ③元素X的最高价氧化物的水化物一定是强酸 ④元素X的气态氢化物分子间一定不能形成氢键.
①元素X 可能是金属元素 ②元素X的气态氢化物一定极易溶于水 ③元素X的最高价氧化物的水化物一定是强酸 ④元素X的气态氢化物分子间一定不能形成氢键.
分析:根据原子核外最外层电子数不超过8可知,2n-1≤8,则n≤4.5,根据n为正整数可分别取值1、2、3、4进行讨论判断,结合元素的性质进行分析.
解答:解:原子核外最外层电子数不超过8可知,2n-1≤8,则n≤4.5,
讨论:n=1,电子层数为1-1=0,不符合题意;
n=2,电子层数为2-1=1,最外层电子数为2×2-1=3,不存在;
n=3时,电子层数为3-1=2,最外层电子数为2×3-1=5,为N元素;
n=4时,电子层数为4-1=3,最外层电子数为2×4-1=7,为Cl元素.
①X为N或Cl,故①错误;
②元素X的气态氢化物为氨气或氯化氢,都极易溶于水,故②正确;
③元素X的最高价氧化物的水化物为硝酸或高氯酸,为强酸,故③正确;
④NH3分子间能形成氢键,④错误.
故选B.
讨论:n=1,电子层数为1-1=0,不符合题意;
n=2,电子层数为2-1=1,最外层电子数为2×2-1=3,不存在;
n=3时,电子层数为3-1=2,最外层电子数为2×3-1=5,为N元素;
n=4时,电子层数为4-1=3,最外层电子数为2×4-1=7,为Cl元素.
①X为N或Cl,故①错误;
②元素X的气态氢化物为氨气或氯化氢,都极易溶于水,故②正确;
③元素X的最高价氧化物的水化物为硝酸或高氯酸,为强酸,故③正确;
④NH3分子间能形成氢键,④错误.
故选B.
点评:本题考查原子结构和元素周期律的关系,题目难度中等,注意结合电子层数和最外层电子数进行讨论解答.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
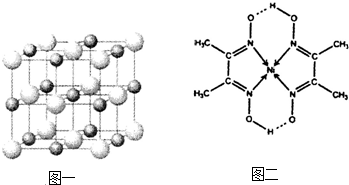 (3)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图一所示),其中3种离子晶体的晶格能数据如下表:
(3)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图一所示),其中3种离子晶体的晶格能数据如下表:
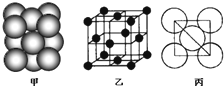
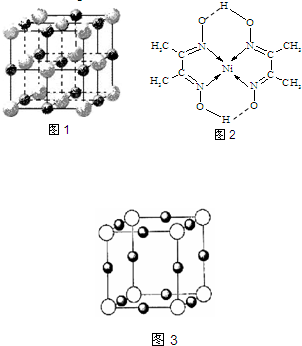 确定物质性质的重要因素是物质结构.请回答下列问题.
确定物质性质的重要因素是物质结构.请回答下列问题.