题目内容
15.甲醇和氧气以及强碱作电解质溶液新型手机电池,电量可达到现在用镍氢或锂电池的十倍,可连续使用一个月才充一次电.该电池反应的离子方程式是:2CH3OH+3O2+4OH-═2CO32-+6H2O.据此判断下列说法正确( )| A. | CH3OH在负极上失去电子,O2在正极上得到电子 | |
| B. | 溶液中OH-向正极移动,H+向负极移动 | |
| C. | CH3OH发生还原反应,O2发生氧化反应 | |
| D. | 随着电极反应的不断进行,电解质溶液的pH值基本保持不变 |
分析 该燃料电池放电时,负极上甲醇失电子发生氧化反应,电极反应式为CH3OH+8OH--6e-═CO32-+6H2O,正极氧气得电子发生还原反应,反应式为O2+2H2O+4e-=4OH-,阳离子移向正极,阴离子移向负极,以此解答该题.
解答 解:A.该燃料电池放电时,负极上甲醇失电子发生氧化反应,电极反应式为CH3OH+8OH--6e-═CO32-+6H2O,正极氧气得电子发生还原反应,反应式为O2+2H2O+4e-=4OH-,故A正确;
B.该燃料电池放电时,阳离子移向正极,阴离子移向负极,所以OH-向负极移动,H+向正极移动,故B错误;
C.放电时,CH3OH参与反应的电极为负极,失电子发生氧化反应,正极氧气得电子发生还原反应,故C错误;
D.该燃料电池放电时,反应为2CH3OH+3O2+4OH-═2CO32-+6H2O,消耗氢氧根,则pH值减小,故D错误.
故选A.
点评 本题考查了燃料电池,燃料电池中负极上燃料发生氧化反应、正极上氧化剂发生还原反应,难点是电极反应式的书写,要根据电解质溶液酸碱性书写电极反应式,题目难度不大.

练习册系列答案
相关题目
6.赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿按一定比例混合加热可制得铜:2Cu2O+Cu2S $\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑.对于该反应,下列说法中正确的是( )
| A. | 该反应中的氧化剂只有Cu2O | |
| B. | 氧化产物和还原产物的物质的量之比为6:1 | |
| C. | Cu既是氧化产物又是还原产物 | |
| D. | Cu2S在反应中既是氧化剂又是还原剂 |
3.电解稀H2SO4、CuCl2的混合液,最初一段时间阴极和阳极上分别析出的物质分别是( )
| A. | H2和Cl2 | B. | Cu和 Cl2 | C. | H2和O2 | D. | Cu和O2 |
10.CO2的资源化利用是解决温室效应的重要途径.以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应: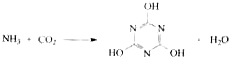 下列有关三聚氰胺的说法正确的是( )
下列有关三聚氰胺的说法正确的是( )
 下列有关三聚氰胺的说法正确的是( )
下列有关三聚氰胺的说法正确的是( )| A. | 分子式为C3H6N3O3 | B. | 分子中既含极性键,又含非极性键 | ||
| C. | 属于共价化合物 | D. | 生成该物质的上述反应为中和反应 |
20.下列措施或事实不能用勒夏特列原理解释的是( )
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | H2、I2、HI平衡混合气减小压强(扩大体积)可使颜色变浅 | |
| C. | 打开汽水瓶盖,有气泡冒出 | |
| D. | 在合成氨的反应中,加压有利于氨的合成 |
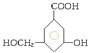
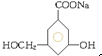
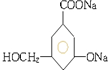
7.下列各有机物的系统命名正确的是( )
| A. | 2,3,3-三甲基丁烷 | B. | 2-乙基丙烷 | ||
| C. | 2-甲基-2-丁烯 | D. | 2,2-二甲基-1,3-丁二烯 |
 .
. .
.