题目内容
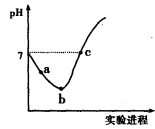
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol·L—1的NaOH溶液。整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是

| A.实验进程中可用pH试纸测定溶液的pH |
B.c点所示溶液中: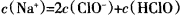 |
| C.向a点所示溶液中通入SO2,溶液的酸性和漂白性均增强 |
D.由a点到b点的过程中,溶液中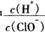 减小 减小 |
B
试题分析:根据题意知,整个过程发生的反应为Cl2+H2O═HCl+HClO、HCl+NaOH═NaCl+H2O、HClO+NaOH═NaClO+H2O。A、实验进程中溶液中有次氯酸生成,具有漂白性,不能用pH试纸测定溶液的pH,错误;B、c点溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(H+)+c(Na+)=c(Cl-)+c(ClO-)+c(OH-),所以c(Na+)=c(Cl-)+c(ClO-),根据物料守恒得c(Cl-)=c(ClO-)+c(HClO),所以c(Na+)=2c(ClO-)+c(HClO),正确;C、向a点所示溶液中通入SO2,发生的反应为:Cl2+SO2 +2H2O====H2SO4 +2HCl,溶液的酸性增强,但漂白性减弱,错误;D、由a点到b点的过程中,溶液中
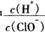 增大,错误。
增大,错误。
练习册系列答案
相关题目
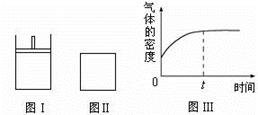
 a Z(g)。
a Z(g)。 3C(s) + 4NH3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示:
3C(s) + 4NH3(g) ΔH>0,在700℃,CH4与N2在不同物质的量之比[n(CH4)/n(N2)]时CH4的平衡转化率如下图所示: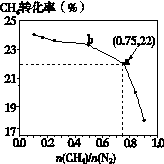
 pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
 CH3OH(g)
CH3OH(g)
 2Z(g) ΔH>0
2Z(g) ΔH>0