题目内容
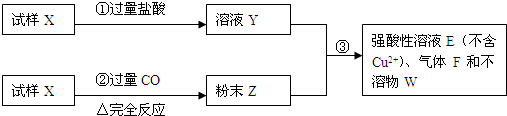
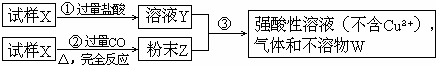
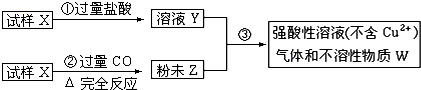
试样X由氧化亚铁和氧化铜组成,取质量相等的两份试样进行图2-4所示实验:
图2-4
(1)写出步骤③发生的全部反应的离子方程式。
(2)若Y和Z充分反应,生成的不溶物的质量是m,则每份试样X中氧化铜为多少克?(用m表示)
解析:本题第(1)问比较简单,发生的反应为:Fe+Cu2+![]() Fe2++Cu,Fe+2H+
Fe2++Cu,Fe+2H+![]() Fe2++H2↑。
Fe2++H2↑。
第(2)问考查思维的严密性和敏捷性。由题意,反应后溶液中不含Cu2+,所以两份试样中的铜元素全部转化为单质铜,而溶液是强酸性,则固体物中无Fe,所以m为铜的质量。故一份试样中氧化铜的质量为 ×M(CuO)=
×M(CuO)=![]() m=58m。
m=58m。
答案:(1)Fe+Cu2+![]() Fe2++Cu Fe+2H+
Fe2++Cu Fe+2H+![]() Fe2++H2↑
Fe2++H2↑
(2)①m为全部Cu的质量
Cu — CuO
64 80
m x=![]()
则每份试样中CuO的质量为![]() 。
。

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目