��Ŀ����
����Ӧ����㷺�Ľ���������±���������������Լ������ĺ������ξ�Ϊ��Ҫ�����
��1����ʵ�����У�FeCl2�������ۺ����ᷴӦ�Ʊ���FeCl3�������ۺ�______��Ӧ�Ʊ�������һ����FeCl2��FeCl3�Ļ�������Ʒ�������Ʒ��n��Fe���sn��Cl��=1�s2.3�������Ʒ��FeCl3�����ʵ�������Ϊ______��
��2��Ҫȷ������ij�Ȼ���FeClx�Ļ�ѧʽ���������ӽ������к͵ζ��ķ�����ʵ���г�ȡ1.08gFeClx��Ʒ���ܽ���Ƚ��������ӽ���Ԥ��������ͨ�����б���OH-�������ӽ�������ʹCl-��OH-����������������ɺ�������Һ��OH-��0.80mol?L-1������ζ��кͣ�ǡ���к�ʱ��������25.0mL������FeClx�е�xֵ��______����ʽ�����㣩
��3�������£�Fe��ˮ������Ӧ�Ļ�ѧ����ʽΪ______��
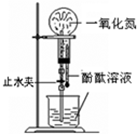
��4�������������Ȼ�������Һ�����ʵ���Ҿ��ױ��ʣ����ֺ��ɫ����������Һ�����ɫ����˷�Ӧ�����ӷ���ʽΪ______��
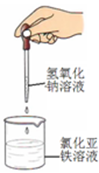
��5�����Ȼ�������Һ�м�������ʵ����Ĺ������ƣ�������Ӧ���ܵ����ӷ���ʽΪ��______��
��1����ʵ�����У�FeCl2�������ۺ����ᷴӦ�Ʊ���FeCl3�������ۺ�______��Ӧ�Ʊ�������һ����FeCl2��FeCl3�Ļ�������Ʒ�������Ʒ��n��Fe���sn��Cl��=1�s2.3�������Ʒ��FeCl3�����ʵ�������Ϊ______��
��2��Ҫȷ������ij�Ȼ���FeClx�Ļ�ѧʽ���������ӽ������к͵ζ��ķ�����ʵ���г�ȡ1.08gFeClx��Ʒ���ܽ���Ƚ��������ӽ���Ԥ��������ͨ�����б���OH-�������ӽ�������ʹCl-��OH-����������������ɺ�������Һ��OH-��0.80mol?L-1������ζ��кͣ�ǡ���к�ʱ��������25.0mL������FeClx�е�xֵ��______����ʽ�����㣩
��3�������£�Fe��ˮ������Ӧ�Ļ�ѧ����ʽΪ______��
��4�������������Ȼ�������Һ�����ʵ���Ҿ��ױ��ʣ����ֺ��ɫ����������Һ�����ɫ����˷�Ӧ�����ӷ���ʽΪ______��
��5�����Ȼ�������Һ�м�������ʵ����Ĺ������ƣ�������Ӧ���ܵ����ӷ���ʽΪ��______��
��1������������ȼ�������Ȼ�����
FeCl2��FeCl3�Ļ�������Ʒ��FeCl2���ʵ���Ϊx��FeCl3�����ʵ���Ϊy����x+y������2x+3y��=1��2.3���õ�x��y=7��3��
�Ȼ������ʵ�������=
��100%=30%��
�ʴ�Ϊ��������30%��
��2��n��Cl��=n��H+��=n��OH-��=0.0250L��0.80mol?L-1=0.020mol��1.08g FeClx��Ʒ�к������������ʵ���Ϊ
��3=0.020 mol�����x=3��
�ʴ�Ϊ��n��Cl��=n��H+��=n��OH-��=0.0250L��0.80mol?L-1=0.020mol��1.08g FeClx��Ʒ�к������������ʵ���Ϊ
��3=0.020 mol�����x=3��
��3�������£�����ˮ������Ӧ������������������������Ӧ����ʽΪ��4H2O��g��+3Fe
Fe3O4+4H2��
�ʴ�Ϊ��4H2O��g��+3Fe
Fe3O4+4H2��
��4���������Ӳ��ȶ��ױ������������������ӣ���������ˮ�����������������������������ױ������������������������������ӷ���ʽ�ֱ�Ϊ��4Fe2++O2+4H+=4Fe3++2H2O��Fe2++2H2O?Fe��OH��2+2H+��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe2++O2+4H+=4Fe3++2H2O��Fe2++2H2O?Fe��OH��2+2H+��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��5���������ƺ�ˮ��Ӧ�����������ƺ��������������ƺ��������ӷ�Ӧ�����������������������������������������������������Է�Ӧ����ʽΪ��4Na2O2+4FeCl2+6H2O=4Fe��OH��3��+8NaCl+O2����
�ʴ�Ϊ��4Na2O2+4FeCl2+6H2O=4Fe��OH��3��+8NaCl+O2����
FeCl2��FeCl3�Ļ�������Ʒ��FeCl2���ʵ���Ϊx��FeCl3�����ʵ���Ϊy����x+y������2x+3y��=1��2.3���õ�x��y=7��3��
�Ȼ������ʵ�������=
| 3 |
| 7+3 |
�ʴ�Ϊ��������30%��
��2��n��Cl��=n��H+��=n��OH-��=0.0250L��0.80mol?L-1=0.020mol��1.08g FeClx��Ʒ�к������������ʵ���Ϊ
| 1.08g |
| (56+35.5x)g/mol |
�ʴ�Ϊ��n��Cl��=n��H+��=n��OH-��=0.0250L��0.80mol?L-1=0.020mol��1.08g FeClx��Ʒ�к������������ʵ���Ϊ
| 1.08g |
| (56+35.5x)g/mol |
��3�������£�����ˮ������Ӧ������������������������Ӧ����ʽΪ��4H2O��g��+3Fe
| ||
�ʴ�Ϊ��4H2O��g��+3Fe
| ||
��4���������Ӳ��ȶ��ױ������������������ӣ���������ˮ�����������������������������ױ������������������������������ӷ���ʽ�ֱ�Ϊ��4Fe2++O2+4H+=4Fe3++2H2O��Fe2++2H2O?Fe��OH��2+2H+��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
�ʴ�Ϊ��4Fe2++O2+4H+=4Fe3++2H2O��Fe2++2H2O?Fe��OH��2+2H+��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��5���������ƺ�ˮ��Ӧ�����������ƺ��������������ƺ��������ӷ�Ӧ�����������������������������������������������������Է�Ӧ����ʽΪ��4Na2O2+4FeCl2+6H2O=4Fe��OH��3��+8NaCl+O2����
�ʴ�Ϊ��4Na2O2+4FeCl2+6H2O=4Fe��OH��3��+8NaCl+O2����

��ϰ��ϵ�д�
 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
�����Ŀ
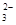 = 2I����S4O
= 2I����S4O