题目内容
20.用双线桥表示下列氧化还原反应电子转移:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O.
分析 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中Mn元素化合价降低,被还原,KMnO4为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂.
解答 解:2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中Mn元素化合价降低,被还原,KMnO4为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂,反应中Mn得到2×5e-,Cl失去10e-,电子转移数目和方向可表示 ,
,
故答案为: .
.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,为高频考点,注意把握元素化合价的变化,能会用双线桥法表示电子转移的方向和数目,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 | |
| C. | 硅材料广泛用于光纤通讯 | |
| D. | 工业上电解熔融的MgCl2,可制得金属镁 |
8.下列说法正确的是( )
| A. | 同温、同压下,相同质量的气体都占有相同的体积 | |
| B. | 同温、同压下,相同体积的气体都含有相同数目的分子 | |
| C. | 在标准状况下,1 mol水的体积约是22.4 L | |
| D. | 1 mol某气体的体积约为22.4 L,该气体所处的状况一定是标准状况 |
15.下列溶液中Cl-的物质的量浓度最大的是( )
| A. | 30mL 0.2mol/L KCl溶液 | B. | 20mL 0.1mol/L CaCl2溶液 | ||
| C. | 100mL 0.25mol/L NaCl溶液 | D. | 10mL 0.1mol/L AlCl3溶液 |
5.汽车安全气囊是在发生撞车时、产生二次碰撞前能够自动膨胀保护乘员的装置,碰撞时发生反应:10NaN3+2KNO3═K2O+5Na2O+16N2↑.下列判断正确的是( )
| A. | N2既是氧化剂又是还原剂 | |
| B. | NaN3中N元素被还原 | |
| C. | 每生成16molN2转移30mole- | |
| D. | 还原产物与氧化产物质量之比为1:15 |
12.下列气体中.可以用来冷却镁蒸气的是( )
| A. | 空气 | B. | 二氧化碳 | C. | 氧气 | D. | 氩气 |
9.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O | |
| B. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| C. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4 Na++2Cu(OH)2↓+O2↑ |
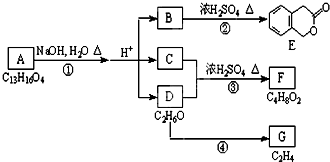 如图中A、B、C、D、E、F、G均为有机化合物.
如图中A、B、C、D、E、F、G均为有机化合物. ;反应①的反应类型是水解反应;
;反应①的反应类型是水解反应; 中任意一种.
中任意一种.