题目内容
7.下列电子式书写正确的是( )| A. | CCl4 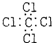 | B. | 氯化镁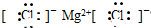 | ||
| C. | 氮气 | D. | 水 |
分析 A.CCl4为共价化合物,氯原子最外层为8个电子;
B.氯化镁是离子化合物,有镁离子和氯离子构成;
C.氮气分子中存在存在2对孤电子对;
D.水为共价化合物,分子中存在2个氢氧共用电子对.
解答 解:A.CCl4为共价化合物,氯原子最外层为8个电子,CCl4正确的电子式为
B.氯化镁是离子化合物,由氯离子和镁离子构成,氯化镁电子式为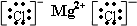 ,故B正确;
,故B正确;
C.氮气分子中存在存在2对孤电子对,氮原子最外层达到8电子稳定结构,氮气正确的电子式为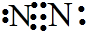 ,故C错误;
,故C错误;
D.水为共价化合物,分子中存在2对氢氧共用电子对,水正确的电子式为
故选B.
点评 本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
相关题目
18.青奥会于2014年8月在南京圆满举行,青奥会建筑设施使用了大量节能材料,体现了“绿色青奥”的理念,下列说法正确的是( )
| A. | 用于青奥村工程隔热保温材料聚氨酯属于有机高分子材料 | |
| B. | 青奥会议中心双塔采用了玻璃幕墙设计,制造玻璃的主要原料为纯碱和石灰石 | |
| C. | 青奥中心外墙的复合保温材料采用铝合金锁边,铝合金比金属铝更具有强度大、耐腐蚀的优点 | |
| D. | 青奥会健身中心的地面采用了聚苯乙烯保温板,聚苯乙烯的结构简式为 |
15.下列说法正确的是( )
| A. | “钡餐”中使用的硫酸钡是弱电解质 | |
| B. | 太阳能电池板中的硅在周期表中处于金属与非金属的交界位置 | |
| C. | 常用的自来水消毒剂有Cl2和二氧化氯,两者都含极性键 | |
| D. | “滴水穿石”不涉及化学变化 |
2.下列有关化学用语,使用正确的是( )
| A. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | NH4Cl的电子式: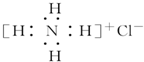 | |
| C. | H、D、T互为同素异形体 | |
| D. | Cl的原子结构示意图: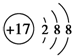 |
12.已知某混合金属粉末,除铝外还含有铁、铜中的一种或两种,所含金属的量都在5%以上.请设计合理实验探究该混合物金属粉末中铁、铜元素的存在.仅限选择的仪器和试剂:烧杯、试管、玻璃棒、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、20%KSCN溶液.
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有Fe(或Cu)元素;
假设2 该混合金属粉末中除铝外还含有Cu(或Fe)元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答).
(3)实验过程
根据(2)的实验方案,完成实验操作、预期现象和结论的有关问题.
完成以下实验探究过程:
(1)提出假设:
假设1 该混合金属粉末中除铝外还含有Fe(或Cu)元素;
假设2 该混合金属粉末中除铝外还含有Cu(或Fe)元素;
假设3 该混合金属粉末中除铝外还含有Fe、Cu元素;
(2)设计实验方案
基于假设3,设计出实验方案(不要在答题卡上作答).
(3)实验过程
根据(2)的实验方案,完成实验操作、预期现象和结论的有关问题.
| 编号 | 实验操作 | 预期现象 | 结论 |
| ① | 用药匙取少许样品,加入试管A中,再用滴管取过量NaOH溶液并滴加到试管A中,充分反应后,静置,弃去上层清液,剩余固体备用 | 样品部分溶解,并有气体放出 | |
| ② | 往试管A的剩余固体中加过量稀硫酸,充分反应后,静置.取上层清液于试管B中,剩余固体备用 | 固体部分溶解,并有气体放出,溶液呈浅绿色 | 可能含铁 (填元素名称,以下同) |
| ③ | 往试管B中加入少许稀硝酸,再滴加KSCN溶液 | 溶液先变黄色,加KSCN后显血红色 | 结合②可知,一定含 |
| ④ | 往②剩余固体中加入稀硝酸,再滴加NaOH溶液 | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色 沉淀产生. | 一定含铜. |
19.氢氧化钡(固体)、硫酸铜(固体)、硫酸(液体)这些物质可以归为一类,下列哪些物质还可以和它们归为一类( )
| A. | 豆浆 | B. | NaCl溶液 | C. | HCl | D. | 空气 |
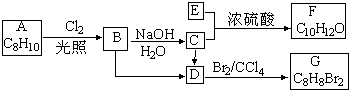
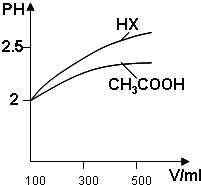 回答下列问题:
回答下列问题: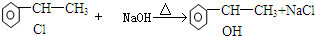 .
.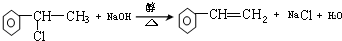 ,E+C→F
,E+C→F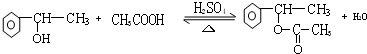
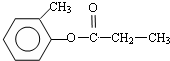
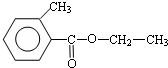
 .
.
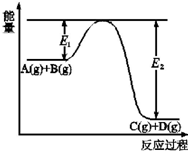 (1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6kJ的热量,试写出对应的热化学方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.标准状况下11.2L氢气在氯气中充分燃烧放出的热量是92.3kJ.
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6kJ的热量,试写出对应的热化学方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.标准状况下11.2L氢气在氯气中充分燃烧放出的热量是92.3kJ.