题目内容
如下图所示,各容器中盛有海水,铁在其中被腐蚀时,由快到慢的顺序是( )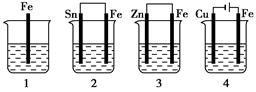
| A.4>2>1>3 | B.2>1>3>4 |
| C.4>2>3>1 | D.3>2>4>1 |
A
解析试题分析:以1作参考。2中构成了原电池,金属活动性Fe>Sn,所以Fe作原电池的负极,Fe反应腐蚀的速率比1快;3中构成了原电池,由于金属活动性Zn>Fe,所以Fe作原电池的正极,首先被你氧化的是Zn,所以Fe被腐蚀的反应速率比1慢;4是电解池,Fe与电源的正极连接,作阳极,发生的反应:Fe-2e-=Fe2+。Fe腐蚀的速率比2快。因此铁在其中被腐蚀时,由快到慢的顺序是4>2>1>3。选项为A.。
考点:考查影响Fe腐蚀的快慢程度的因素知识。

用酸性氢氧燃料电池为电源进行电解的实验装置如下图所示。下列说法正确的是( ) 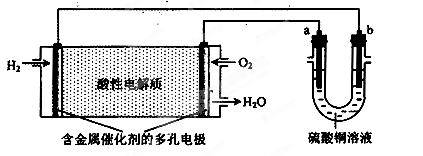
| A.a为负极,b为正极 |
| B.若a极是铁,b极是铜,b极逐渐溶解,a极上有铜析出 |
| C.若a、b极都是石墨,在相同条件下,理论上a极产生的气体与电池中消耗的O2体积相等 |
| D.若电解精炼粗铜时,b极是粗铜,a极是纯铜 |
下列描述中,不符合生产实际的是 ( )
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 | B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 | D.在镀件上电镀锌,用锌作阳极 |
已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。关于标有“+”的接线柱,下列说法中正确的是
| A.充电时作阳极,放电时作负极 | B.充电时作阳极,放电时作正极 |
| C.充电时作阴极,放电时作负极 | D.充电时作阴极,放电时作正极 |
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某型甲醇燃料电池的总反应式2CH4O + 3O2 = 2CO2↑+ 4H2O,下图是该燃料电池的示意图。下列说法错误的是( )
| A.燃料电池将化学能转化为电能 |
| B.a是甲醇、b是氧气 |
| C.质子从M电极区穿过交换膜移向N电极区 |
| D.负极反应:CH4O - 6e- + H2O = CO2↑+ 6H+ |
某课外活动小组,为研究金属的腐蚀和防护的原理,做了以下实验:将剪下的一块镀锌铁片,放入锥形瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞试液,按如图所示的装置进行实验,过一段时间后观察,下列现象不可能出现的是( )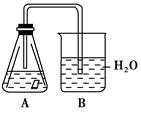
| A.B中导气管中产生气泡 | B.B中导气管里形成一段水柱 |
| C.金属片剪口变红 | D.锌被腐蚀 |
汽车的启动电源常用铅蓄电池。其结构如下图所示,放电时的电池反应如下:PbO2+Pb+2H2SO4=2PbSO4+2H2O根据此反应判断下列叙述中正确的是
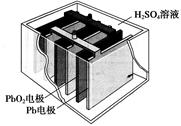
| A.PbO2是电池的负极 |
| B.放电时,溶液中的H+向正极区移动,正极区域的溶液的酸性增强 |
| C.放电时,电子由Pb电极通过导线流向PbO2 |
| D.正极的电极反应式为Pb-2e-=Pb2+ |
下图是研究铁钉腐蚀的装置图,下列说法不正确的是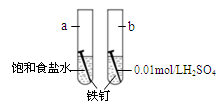
| A.铁钉在两处的腐蚀速率:a < b |
| B.a、b两处铁钉中碳均正极 |
| C.a、b两处铁钉中的铁均失电子被氧化 |
| D.a、b两处的正极反应式均为O2+4e-+4H+ ===2H2O |
某原电池总反应为2Fe3++Fe=3Fe2+,不能实现该反应的原电池是( )
| A.正极为Cu,负极为Fe,电解质溶液为FeCl3 |
| B.正极为C,负极为Fe,电解质溶液为Fe(NO)3 |
| C.正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3 |
| D.正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3 |