题目内容
下列常见金属的冶炼原理中不合理的是( )
| | 金属 | 冶炼原理 |
| A | Fe |  |
| B | Hg | 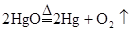 |
| C | Al | 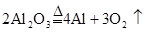 |
| D | Na |  |
C
试题分析:C选项中应为点解熔融状态的氧化铝
2Al2O3(熔融)
 4Al+3O2 ↑
4Al+3O2 ↑ 
练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
题目内容
| | 金属 | 冶炼原理 |
| A | Fe |  |
| B | Hg | 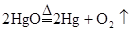 |
| C | Al | 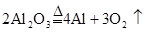 |
| D | Na |  |
 4Al+3O2 ↑
4Al+3O2 ↑ 
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案