题目内容
10.下列有关核外电子排布的式子不正确的是( )| A. | 24Cr的电子排布式:1s22s22p63s23p63d54s1 | |
| B. | K的价电子排布式:4s1 | |
| C. | 氮原子的轨道表示式: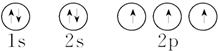 | |
| D. | 硫原子的轨道表示式: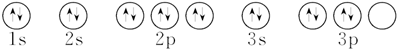 |
分析 A.Cr原子核外有24电子,注意全满半满的稳定结构;
B.K原子的价电子为1;
C.轨道表示式要遵循洪特规则和保利不相容原理;
D.电子总是先单独占据一个轨道,且自旋相同.
解答 解:A.Cr原子核外有24电子,核外电子排布式为1s22s22p63s23p63d54s1,故A正确;
B.K原子的价电子为1,价电子排布式:4s1,故B正确;
C.轨道表示式要遵循洪特规则和保利不相容原理,所以N原子的轨道表示式: ,故C正确;
,故C正确;
D.轨道表示式要遵循洪特规则和保利不相容原理,电子总是先单独占据一个轨道,且自旋相同,故D错误.
故选D.
点评 本题考查化学用语,涉及电子轨道表示式、核外电子排布式,侧重基础知识的考查,难度不大.

练习册系列答案
相关题目
18.某烃在光照的条件下与氯气反应能生成三种不同的一氯代物,1mol它在氧气中充分燃烧,需要消耗氧气212.8L(标准状况下),该烃的结构简式是( )
| A. | 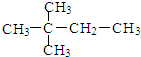 | B. |  | ||
| C. | CH3CH2CH2CH2CH3 | D. | 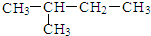 |
15.金刚石和石墨是碳元素的两种结构不同的单质.在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热量.据此,试判断在l00kPa压强下,下列说法正确的是( )
| A. | 金刚石比石墨稳定 | B. | 石墨和金刚石是碳元素的同位素 | ||
| C. | 1mol石墨比1mol金刚石的总能量高 | D. | 金刚石转化为石墨属于化学变化 |
2.下列说法正确的是( )
| A. | 二氧化硫具有还原性 | |
| B. | 因为二氧化硫具有漂白性,能使品红溶液永久褪色 | |
| C. | 大气中二氧化碳浓度高时能形成酸雨 | |
| D. | 浓硫酸常用作干燥剂,因为浓硫酸具有脱水性 |
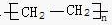 .
. NaCl
NaCl H2O2
H2O2
 NH3:3H•+
NH3:3H•+ →
→ .
.