题目内容
人体血液中存在平衡:CO2 + H2O  H2CO3
H2CO3  HCO3—,使血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。已知pH随c(HCO3—)︰c(H2CO3) 变化关系如下表所示,则下列说法中不正确的是
HCO3—,使血液pH保持在7.35~7.45之间,否则就会发生酸中毒或碱中毒。已知pH随c(HCO3—)︰c(H2CO3) 变化关系如下表所示,则下列说法中不正确的是
| c(HCO3—):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
B.人体发生酸中毒时,可静脉滴注一定浓度的NaHCO3溶液解毒
C.常温下将pH=7.40的血液稀释至pH=7时,c(H+)·c(OH—)一定不变
D.c(HCO3—)︰c(H2CO3)=1时,H2CO3的电离程度小于HCO3—的水解程度
解析试题分析:A、pH=7的血液中,c(HCO3—):c(H2CO3)介于1.0~17.8之间,所以c(HCO3—) > c(H2CO3),正确;B、注射NaHCO3溶液使平衡逆向移动,生成二氧化碳,可以降低体内的酸度,正确;C、水的离子积是温度常数,温度不变,c(H+)·c(OH—)一定不变,正确;D、c(HCO3—)︰c(H2CO3)=1时,pH=6.10,溶液显酸性,H2CO3的电离使溶液显酸性,HCO3—的水解使溶液显碱性,所以H2CO3的电离程度大于HCO3—的水解程度,错误,答案选D。
考点:考查离子浓度的大小比较,化学平衡的移动,电离与水解程度的判断

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的水溶液因发生水解而显酸性的是
| A.NH4Cl | B.KHSO4 | C.NaHCO3 | D.H2SO4 |
一定温度下,将0.1molAgCl加入1L 0.1mol·L-1Na2CO3溶液中,充分搅拌(不考虑液体体积变化),已知:Ksp(AgCl)=2×10-10;Ksp(Ag2CO3)=1×10-11,下列有关说法正确的是
A.沉淀转化反应2AgCl(s)+ CO32-(aq) Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol·L-1 Ag2CO3(s)+2Cl-(aq)的平衡常数为20mol·L-1 |
| B.约有2×10-5mol AgCl溶解 |
| C.反应后溶液中的:c(Na+)>c (Cl-) >c (CO32-) >c (OH-) >c (H+) |
| D.反应后溶液中的:c(Na+)+ c (H+)+ c (Ag+)="2" c (CO32-)+ c (HCO3-)+ c (Cl-)+ c (OH-) |
25℃时,下列说法正确的是( )
| A.氨水与氯化铵的pH=7的混合溶液中:c(Cl—)>c(NH4+) |
| B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3—) >c(H2CO3)>c(CO32?) |
| C.pH=12的NaOH溶液与等体积pH=2的醋酸溶液混合后所得溶液显酸性 |
| D.将0.1 mol/L的氨水溶液加水稀释10倍,溶液中离子浓度都减少 |
下列说法正确的是
| A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4 |
| B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol/L NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1 mol/L),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol/L盐酸、③0.1 mol/L氯化镁溶液、④0.1mol/L硝酸银溶液中,Ag+浓度:①>④=②>③ |
污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀。下列物质不能作为沉淀剂的是
| A.氨水 | B.硫化氢气体 |
| C.硫酸钠溶液 | D.纯碱溶液 |
有关AgCl的沉淀溶解平衡的说法正确的是
| A.AgCl沉淀生成和溶解同时在不断进行,且速率相等 |
| B.AgCl难溶于水,溶液中没有Ag+和Cl- |
| C.用等体积的蒸馏水和0.01mol·L-1的盐酸洗涤AgCl沉淀,用水洗涤造成的AgCl的损失小于用稀盐酸洗涤的损失量。 |
| D.向含有AgCl的悬浊液中加入NaBr固体,AgCl沉淀不变化 |
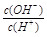 =1×10-8,下列叙述正确的是( )
=1×10-8,下列叙述正确的是( )