��Ŀ����
��ͼÿһ�����е���ĸ����һ�ַ�Ӧ��������

��1����X��M��N���ֶ�������ͬ����Ԫ���γ� ��Mԭ�ӵ����������������ڲ��������![]() NԪ��������������ĸ��۴�����Ϊ6��
NԪ��������������ĸ��۴�����Ϊ6��
��д����Ӧ������ӷ���ʽ ��
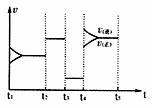
����ͼΪIV�ﵽƽ���ı䷴Ӧ��������Ӧ������ʱ��仯���������֪t2-t3��Ϊ���ô�����t3-t4��Ϊ��С��ϵ��ѹǿ��д���������������Ļ�ѧ����ʽ ��дһ�����ɣ��þ������ʱ�ʾ������t4-t5��Ϊ������ϵ���¶ȣ���÷�ӦΪ ������ȡ������ȡ���
��ij�¶��£��ĸ������о�������������Ӧ�������ʵ����ʵ���Ũ�ȼ����淴Ӧ���ʹ�ϵ���±���ʾ������д������Ӧ�Ŀո�
| ������� | C(C)/mol?L�D1 | C(D)/mol?L�D1 | C(G)/mol?L�D1 | V����V���Ƚ� |
| �� | 0.06 | 0.60 | 0.60 | V��=V�� |
| �� | 0.6 | 0.50 | 0.40 | |
| �� | 0.12 | 0.40 | 0.80 | V��<V�� |
| �� | 0.12 | 0.30 | V��=V�� |
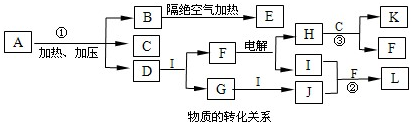
��2����X��һ�ֺ������Σ�B�ǽ������ʣ�C��D�Ƿǽ������ʣ���Ӧ����ҪB��A��Ũ��Һ���Ȳ��ܽ��У������ɵ�E��G��ͬһ�����ʡ�д����Ӧ��Ļ�ѧ����ʽ ��4g��̬D��C����ȫ��Ӧ�ų�37.2kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��1����C12+2OH�D C1�D+C1O�D+H2O
��H2��g��+I2��g�� 2HI��g�� ����
��V��>V�� 0.60
��2��2CuSO4+2H2O![]() 2Cu+O2��+2H2SO4
2Cu+O2��+2H2SO4
S��s��+O2��g�� SO2��g�� ��H=��297.6mol�D1


 NH4++NH2-
NH4++NH2-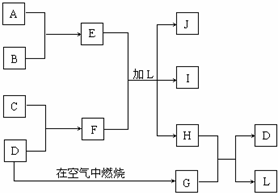 ��ͼÿһ�����е���ĸ����һ�ַ�Ӧ��������
��ͼÿһ�����е���ĸ����һ�ַ�Ӧ��������
