题目内容
【题目】下图表示有关物质之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物(反应条件图中已省略)
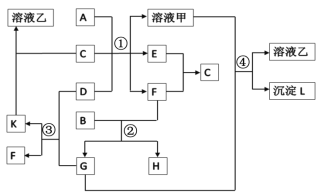
(1)A,D代表的物质分别为:________,________(填化学式);
(2)反应①中的C,D均过量,该反应的化学方程式是____________________________________;
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是_______,_______(填化学式);其物质的量之比为__________.
(4)反应③产物中K的化学式为____________;④的离子方程式为_____________________________.
【答案】Al Na2O2 2H2O +Na2O2 =4NaOH+O2↑、2Al+ 2NaOH+2H2O=2NaAlO2+3H2↑ CO2 CO 1:1 Na2CO3 2![]() +CO2+3H2O=2Al(OH)3↓+
+CO2+3H2O=2Al(OH)3↓+![]()
【解析】
题干信息,A为常见的金属单质,B为非金属单质(一般是黑色粉末)推断为C,C是常见的无色无味液体可以推断为H2O,D是淡黄色的固体化合物判断为Na2O2,E、F为O2和H2的反应生成水,A是常见金属,与另一种固体在水中反应生成O2和H2,则该固体金属为Al,固体D为Na2O2,能与水和CO2反应,则G为CO2;说明K为Na2CO3,F为O2; 题给信息黑色单质B与氧气(F)反应得到G(CO2),说明B为C(碳),C和O2反应可生成CO2和CO,则H为CO;依据F(O2)与E反应生成C(水)可知E为氢气,结合物质的性质解答该题。
推断可知A为Al,B为C,C为H2O,D为Na2O2,E为H2,F为O2,G为CO2,H为CO,K为Na2CO3;
(1) 依据推断可知,A、D代表的物质分别为:Al、Na2O2;
(2) 反应①中的C、D均过量,生成的氢氧化钠溶液能和A完全反应,该反应的化学方程式是:2H2O+2Na2O2=4NaOH+O2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3) 依据反应C+O2=CO2:n(C):n(O2)=1:1,发生反应产物为二氧化碳;依据反应2C+O2=2CO;n(C):n(O2)=2:1,发生反应生成一氧化碳气体;反应②中,若B(C)与F(O2)物质的量之比为4:3,1:1<n(C):n(O2)=4:3<2:1;判断G、H分别是:CO2、CO;设CO2的物质的量为amol、CO的物质的量为bmol,则a+b=4、2a+b=6,解得:a=2、b=2,故CO2和CO物质的量之比为2mol:2mol=1:1;
(4) 反应③是过氧化钠和二氧化碳气体的反应生成碳酸钠和氧气,F为氧气,产物中K为碳酸钠,化学式为:Na2CO3;分析判断G为CO2,溶液乙是碳酸钠溶液,G+溶液甲=溶液乙+沉淀L,所以甲溶液中的偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,反应④的离子方程式为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-。