题目内容
【题目】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
(1)SO2(g)+2CO(g)2CO2(g)+S(l)△H<0
①如果要提高上述反应的反应速率,可以采取的措施是 . (选填编号)
a.减压 b.增加SO2的浓度 c.升温 d.及时移走产物
②若反应在恒容的密闭绝热容器中进行,下列说法不正确的是 . (选填编号)
a.平衡前,随着反应的进行,容器内压强始终不变
b.当容器内温度不再变化时,反应达到了平衡
c.其他条件不变,升高温度可增大平衡常数
d.其他条件不变,使用不同催化剂,该反应热效应不同
③该反应的平衡常数表达式是′;某温度下2L恒定容器中加入2mol的SO2和2mol的CO.10分钟内,气体密度减小了8g/L,则CO的反应速率是 .
(2)SO2(g)+NO2(g)NO(g)+SO3(g)
①在2L恒定容器中加入2mol的SO2和2mol的NO2 , 达到平衡时测得SO2的转化率为50%,向该容器中再加入1mol的SO2 , 平衡将向方向移动,计算重新达到平衡时SO2的浓度是 , SO2的转化率由50%变为 , NO2的转化率由变为 .
②实验结果启示我们:增大一种反应物浓度,其转化率将(填增大、减小或不变),另一种反应物的转化率将 . 现实生产的意义是:可以通过增大的用量,来提高成本高的反应物的利用率.
【答案】
(1)bc;acd;0.05mol/(L﹒min)
(2)正;0.9mol/L;40%;50%;60%;减小;增大;低成本物质
【解析】解:(1)①a.减压,减小速率,故错误; b.增加SO2的浓度,加快反应速率,故正确;
c.升温,加快反应速率,故正确;
d.及时移走产物,相对于减小浓度,减小反应速率,故错误;
所以答案是:bc;②a.平衡前,随着反应的进行,气体的物质的量减小,故容器内压强始会减小,故错误;
b.温度为变量,当容器内温度不再变化时,反应达到了平衡,故正确;
c.平衡时,其他条件不变,正反应是放热反应,所以升高温度K减小,故错误;
d.反应热效应与催化剂无关,故错误;
所以答案是:acd;③根据平衡常数的定义书写表达式为:K= ![]() ,2L容器中,10分钟内,气体密度减小了8g/L,则减少的S为0.25mol/L,变化的CO的浓度为0.5mol/L,故CO的反应速率是0.05mol/(L﹒min),所以答案是:
,2L容器中,10分钟内,气体密度减小了8g/L,则减少的S为0.25mol/L,变化的CO的浓度为0.5mol/L,故CO的反应速率是0.05mol/(L﹒min),所以答案是: ![]() ;0.05mol/(L﹒min);(2)①在2L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,转化的SO2为2mol×50%=1mol,则:
;0.05mol/(L﹒min);(2)①在2L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,当达到平衡状态时,测得容器中SO2(g)的转化率为50%,转化的SO2为2mol×50%=1mol,则:
SO2(g)+NO2(g)SO3(g)+NO(g)
起始量(mol):2 2 0 0
转化量(mol):1 1 1 1
平衡量(mol):1 1 1 1
平衡常数K= ![]() =
= ![]() =1
=1
再继续加入1mol的SO2(g),等效为开始加入3mol的SO2(g)和2mol的NO2(g),设平衡时容器中SO2(g)的浓度是xmol/L,则:
SO2(g)+NO2(g)SO3(g)+NO(g)
起始量(mol/L):1.5 1 0 0
转化量(mol/L):1.5﹣x 1.5﹣x 1.5﹣x 1.5﹣x
平衡量(mol/L):x x﹣0.5 1.5﹣x 1.5﹣x
所以 ![]() =1,解得x=0.9mol/L,
=1,解得x=0.9mol/L,
SO2、NO2起始物质的量之比为1:1,又按物质的量1:1反应,二者转化率相等,故NO2的转化率为50%;新平衡时SO2的转化率= ![]() ×100%=40%、NO2的转化率=
×100%=40%、NO2的转化率= ![]() ×100%=60%;
×100%=60%;
所以答案是:正;0.9mol/L;40%;50%;60%;②增大一种反应物的用量,其转化率将减小,另一反应物的转化率将增大,现实生产中的意义是:可以通过增大低成本物质的用量,来提高成本高的反应物的利用率,
所以答案是:减小;增大;低成本物质.
【考点精析】认真审题,首先需要了解化学平衡状态本质及特征(化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)),还要掌握化学平衡的计算(反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%)的相关知识才是答题的关键.

【题目】(12分)
CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:
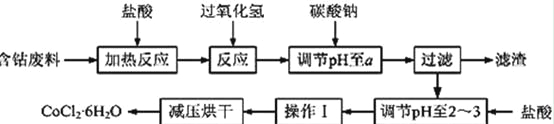
已知:
①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴。
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为 。
(2)加入碳酸钠调节pH至a,a的范围是 ;
(3)操作Ⅰ包含3个基本实验操作,它们是 、 和过滤。
(4)制得的CoCl2·6H2O需减压烘干的原因是 。
(5)为测定产品中CoCl2·6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量。通过计算发现产品中CoCl2·6H2O的质量分数大于100%,其原因可能是 (任写1点)。