题目内容
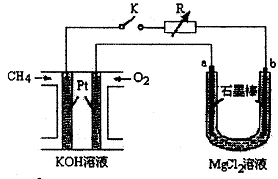
在25℃时,用石墨电极电解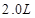 ,
, 溶液,如有
溶液,如有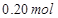 电子发生转移,试回答下列问题:
电子发生转移,试回答下列问题:
(1)阴极发生 反应,电极反应为 。
(2)阳极发生 反应,电极反应为 。
(3)电解后得到的 的质量是 ,得到
的质量是 ,得到 的体积(标准状况)是 。
的体积(标准状况)是 。
(4)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差 ,电解液的 (填“变小”、“变大”或“不变”)
(填“变小”、“变大”或“不变”)
(1)还原 Cu2++2e-=Cu (2)氧化 4OH--4e-=2H2O+O2↑
(3)6.4g 1.12L (4)12.8g 不变
解析试题分析:(1)惰性电极电解硫酸铜溶液,阴极发生还原反应,则溶液中的铜离子在阴极得到电子而析出,电极反应式是Cu2++2e-=Cu。
(2)惰性电极电解硫酸铜溶液,阳极失去电子,发生氧化反应。则溶液中的OH-放电生成氧气,电极反应式是4OH--4e-=2H2O+O2↑。
(3)反应中注意0.20mol电子,则根据反应式Cu2++2e-=Cu可知,析出0.10mol铜,质量是6.4g。根据反应式4OH--4e-=2H2O+O2↑可知,生成氧气的物质的量是0.05mol,标准状况下的体积是0.05mol×22.4L/mol=1.12L。
(4)如用等质量的两块铜片代替石墨作电极,则阳极是铜失去电子,质量减少6.4g。阴极是溶液中的铜离子得到电子,析出6.4g铜,所以电解后两铜片的质量相差12.8g,而溶液中的浓度不变,则pH不变。
考点:考查电解池的有关判断和计算
点评:该题是高考中的常见题型,属于中等难度的试题。该题的关键是明确电解池的工作原理,并依据电子得失守恒计算,然后结合题意灵活运用即可。有利于培养学生的逻辑推理能力和规范的答题能力。

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案某小组同学以碳棒为电极电解CuCl2溶液时,发现阴极碳棒上除了有红色物质析出外,还有少量白色物质析出。为探究阴极碳棒上的产物,同学们阅读资料并设计了如下过程:
Ⅰ.有关资料:铜的化合物颜色性质如下
| 物质 | 颜色、性质 | 物质 | 颜色、性质 |
| 氢氧化铜Cu(OH)2 | 蓝色固体不溶于水 | 硫酸铜(CuSO4) | 溶液呈蓝色 |
| 氧化亚铜(Cu2O) | 红色固体不溶于水 | 氯化铜(CuCl2) | 浓溶液呈绿色,稀溶液呈蓝色 |
| 氯化亚铜(CuCl) | 白色固体不溶于水 | 碱式氯化铜 | 绿色固体不溶于水 |
Ⅱ.探究实验:
(1)提出假设
①红色物质一定有铜,还可能有Cu2O;
②白色物质为铜的化合物,其化学式可能为__________________________。
(2)实验验证
取电解CuCl2溶液后的阴极碳棒,洗涤、干燥,连接下列装置进行实验,验证阴极产物,
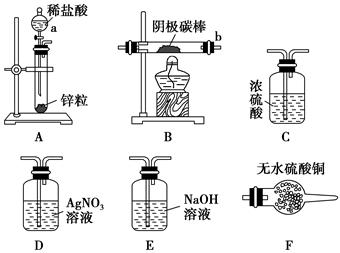
①实验前,检查装置A气密性的方法是_______________________________。
②实验时,各装置从左至右的连接顺序为A→________→________→B→________→________。
(3)观察现象,得出结论
实验结束后,碳棒上的白色物质变为红色,F中物质不变色,D中出现白色沉淀,根据现象①碳棒上的红色物质是否有Cu2O________(填“是”或“否”),理由是________________________________________________________;
②装置________(填上图中装置编号)中________的现象说明提出假设②中的白色物质一定存在;
③写出装置B中发生反应的化学方程式___________________________ _。
(4)问题讨论
①电解CuCl2溶液后的阴极上发生的反应为:______________________
和_______________________________________________________________;
②实验过程中,若装置B中的空气没有排净就开始加热,可能对实验造成的影响是__________________________________________________________。
有两种气态烷烃的混合物,在标准状况下,密度为1.16g/L,则下列关于此混合物组成的说法正确的是
| A.一定有甲烷 | B.一定有乙烷 |
| C.可能是甲烷和戊烷的混合物 | D.可能是乙烷和丙烷的混合物 |






 2CO2(g)+ N2(g)△H <0
2CO2(g)+ N2(g)△H <0
 N2O4(g) △H=-56.9 kJ/mol ②
N2O4(g) △H=-56.9 kJ/mol ②