题目内容
溴水中存在着如下的平衡:Br2+H2O?HBr+HBrO,下列措施,不能使溶液颜色变浅的是( )
| A、通入乙烯气体 |
| B、通入SO2气体 |
| C、加入NaF晶体 |
| D、加入NaI晶体 |
考点:化学平衡的影响因素,氯、溴、碘及其化合物的综合应用
专题:化学平衡专题,卤族元素
分析:若要使溴水的颜色变浅,可以通过改变条件使化学平衡向正反应方向移动,也可能加入能和溴发生反应的某些物质,结合溴的性质分析解答.
解答:
解:A.乙烯气体与溴水发生加成反应,所以使溴水颜色变浅,故A不选;
B.通入二氧化硫,溴具有强氧化性,在水溶液溴能氧化二氧化硫生成硫酸,自身被还原生成氢溴酸,所以能使溴水颜色变浅,故B不选;
C.加入氟化钠晶体,氢溴酸的酸性大于氢氟酸,所以氢溴酸和氟化钠反应,促进平衡向正反应方向移动,所以能使溴水颜色变浅,故C不选;
D.加入NaI晶体,与溴水发生置换反应生成紫色的碘颜色变深,故选D;
故选D.
B.通入二氧化硫,溴具有强氧化性,在水溶液溴能氧化二氧化硫生成硫酸,自身被还原生成氢溴酸,所以能使溴水颜色变浅,故B不选;
C.加入氟化钠晶体,氢溴酸的酸性大于氢氟酸,所以氢溴酸和氟化钠反应,促进平衡向正反应方向移动,所以能使溴水颜色变浅,故C不选;
D.加入NaI晶体,与溴水发生置换反应生成紫色的碘颜色变深,故选D;
故选D.
点评:本题考查了氧化还原反应、化学平衡移动,明确物质的性质是解本题关键,易错选项是B,注意二氧化硫能和溴发生氧化还原反应而使化学平衡移动,为易错点.

练习册系列答案
相关题目
下列有机物的命名正确的是( )
| A、3,3-二甲基丁烷 |
| B、3-甲基-2-乙基戊烷 |
| C、2,3-二甲基-1-戊烯 |
| D、2-甲基-1-戊炔 |
在一定条件下,下列物质不能和二氧化硅反应的是( )
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤硝酸 ⑥氢氧化钾 ⑦氧化钙 ⑧氮气.
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤硝酸 ⑥氢氧化钾 ⑦氧化钙 ⑧氮气.
| A、③⑤⑦⑧ | B、⑤⑦⑧ |
| C、⑤⑧ | D、⑤ |
用铂作电极,KOH溶液作电解质溶液,分别向两极通入CH4和O2,即产生电流,称为甲烷燃料电池.已知甲烷燃料电池的总反应为CH4+2O2+2OH-═CO32-+3H2O,下列有关说法中错误的是( )
| A、CH4在负极上反应 |
| B、放电过程中电解质溶液的碱性不变 |
| C、此电池属于环境友好电池 |
| D、可判断正极反应式为:2O2+8e-+4H2O═8OH- |
有主族元素X、Y,X的原子序数为a,X+比Y2-少8个电子,则Y的原子序数为( )
| A、a+4 |
| B、a+5 |
| C、a+6 |
| D、a+7 |
设NA表示表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1mol NH4+含有的电子数为1NA |
| B、标况下22.4L Cl2溶于水,转移电子数为1NA |
| C、0.1L 3mol/L的NH4NO3溶液中氮原子数等于0.6NA |
| D、3mol NO2溶于水转移电子3mol |
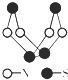 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A、该物质的分子式为SN |
| B、该物质的晶体中微粒间作用力有2种 |
| C、该物质具有很高的熔、沸点 |
| D、该物质与化合物S2N2互为同素异形体 |
下列变化中,属于化学变化的是( )
| A、用苯从溴水中萃取溴 |
| B、重油裂化得到轻质燃料油 |
| C、从煤焦油中提取苯、甲苯、二甲苯 |
| D、石油分馏得到汽油、煤油等产物 |
将a moL/L的Na2CO3溶液与b mol/L的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断不正确的是( )
| A、c(Na+)+c(H+)>c(CO32-)+c(HCO3-)+c(OH-) |
| B、c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、若a=b则可确定c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3) |
| D、若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则一定a<b |