题目内容
5.有机化合物M的结构简式为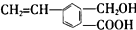 ,关于M的说法正确的是( )
,关于M的说法正确的是( )| A. | M中只有两种官能团 | |
| B. | 1 molM最多能消耗2 mol NaOH | |
| C. | M能使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色 | |
| D. | M可以发生酯化、加成反应,不能发生聚合反应 |
分析 有机物含有碳碳双键,可发生加成、加聚和氧化反应,含有羧基,具有酸性,可发生中和、酯化反应,含有羟基,可发生取代、氧化反应,以此解答该题.
解答 解:A.由结构简式可知分子中含有碳碳双键、羟基、羧基等官能团,故A错误;
B.能与氢氧化钠反应的只有羧基,则1 molM最多能消耗1 mol NaOH,故B错误;
C.碳碳双键可与溴水发生加成反应,可与酸性高锰酸钾发生氧化还原反应,故C正确;
D.含有碳碳双键,可发生聚合反应,故D错误.
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重醇、羧酸、烯烃性质的考查,题目难度中等.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
19.关于化学键的下列叙述中,正确的是( )
| A. | 凡金属元素与非金属元素化合时都能形成离子键 | |
| B. | 非金属原子间不可能形成离子键 | |
| C. | 钠原子与氯原子通过得失电子,以离子键结合成氯化钠后体系能量降低 | |
| D. | 含有共价键的化合物一定是共价化合物 |
10.下列化学用语表示正确的是( )
| A. | HClO的电子式为: | |
| B. | 硝基苯的结构简式为: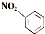 | |
| C. | 含18个中子的氯原子的核素符号:${\;}_{35}^{17}$Cl | |
| D. | 四氯化碳分子比例模型: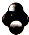 |
17.可用于电动汽车的铝-空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极.下列说法不正确的是( )
| A. | 以NaCl溶液或NaOH溶液为电解液时,正极反应都为O2+2H2O+4e-=4OH- | |
| B. | 以NaOH溶液为电解液时,负极反应为Al+4OH--3e-=AlO2-+2H2O | |
| C. | 以NaOH溶液为电解液时,电池在工作过程中电解液的pH增大 | |
| D. | 以NaCl溶液为电解液时,电流由空气电极沿导线流向铝合金电极 |
14.元素的性质呈周期性变化的根本原因是( )
| A. | 元素的相对原子质量的递增 | |
| B. | 元素的原子半径呈周期性变化 | |
| C. | 元素原子的最外层电子排布呈周期性变化 | |
| D. | 元素的金属性和非金属性呈周期性变化 |
15.二甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能;二甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol;工业上用合成气(CO、H2)直接或间接制取二甲醚.下列叙述正确的是( )
| A. | 以二甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池中负极上的电极反应式为:CH3OCH3-12e-+12OH-═2CO2+8H2O | |
| B. | 二甲醚为不可再生能源 | |
| C. | 二甲醚分子中只含有极性键 | |
| D. | 二甲醚燃烧的热化学方程式表示为:CH3OCH3(g)+3O2(g)═2CO2(g)+3H2O(g);△H=-1455kJ/mol |
