题目内容
【题目】(1)氢气是一种未来十分理想的能源。
镧镍合金是一种良好的储氢材料,在一定条件下通过如下反应实现储氢:
LaNi3(s)+3H2(g) ![]() LaNi3H6(s) H<0。 某实验室模拟该过程,向体积一定的密闭容器中充入反应物发生反应。H2的平衡转化率与其初始加入量(n)、反应温度(T)的关系如下左图所示;一定温度(T)下,将a mol的氢气充入体积是1 L的容器内,气体的压强(P)随时间(t)的变化关系如下右图所示:
LaNi3H6(s) H<0。 某实验室模拟该过程,向体积一定的密闭容器中充入反应物发生反应。H2的平衡转化率与其初始加入量(n)、反应温度(T)的关系如下左图所示;一定温度(T)下,将a mol的氢气充入体积是1 L的容器内,气体的压强(P)随时间(t)的变化关系如下右图所示:

①n1、n2、n3的大小关系是_______。
②温度T1下反应的平衡常数是__________(用含a的代数式表示)。
③保持温度不变,在t6时刻将容积压缩至原容积的一半,容器内的压强_________6kPa(填写“大于”或“小于”)。
(2)贮氢合金ThNi5可催化由CO、H2合成CH4等有机化工产品的反应。温度为TK时发生以下反应①![]()
②![]()
③![]()
![]() _______。
_______。
(3)TK时,向一恒压密闭容器中充入等物质的量的CO(g)和H2O(g)发生上述反应②(已排除其他反应干扰),测得CO(g)物质的量分数随时间变化如下表所示:

若初始投入CO为2 mol,恒压容器容积10 L,用H2O(g)表示该反应0-5分钟内的速率v[H2O(g)]=______。6分钟时,仅改变一种条件破坏了平衡,且第9min达到平衡时,CO的物质的量是0.2mol,则改变的外界条件为_________。
(4)温度、压强对反应CO(g)十2H2(g)=CH3OH(g) H=-90. 1 kJ·mol-1中CO转化率的影响如图所示:

①温度在较低范围内,对CO转化率影响的主要因素是____________ (填“温度”或“压强”)。
②由图像可知,温度越低,压强越大,CO转化率越高。但实际生产往往采用300~400 °C和10 MPa的条件,其原因是________。
【答案】n1<n2<n3 ![]() 小于 -206 kJ·mol-1 0.032mol/L 降低温度 温度 温度太低,反应速率太慢,不利于甲醇的合成,压强太大,设备要求提高,成本增加
小于 -206 kJ·mol-1 0.032mol/L 降低温度 温度 温度太低,反应速率太慢,不利于甲醇的合成,压强太大,设备要求提高,成本增加
【解析】
(1) LaNi3(s)+3H2(g)![]() LaNi3H6(s) H<0。
LaNi3H6(s) H<0。
①该反应是一个气体分子数减小的反应,在恒容密闭容器中进行该反应,充入氢气,相当于增大压强,平衡正向移动,氢气的转化率将增大;
②由图可知,平衡时,体系压强由9kPa变为3kPa,氢气的物质的量变为起始值的三分之一;
③保持温度不变,容积压缩至原容积的一半,平衡正向移动,气体分子数减小,压强应小于起始压强的2倍;
(2)第三个反应出现CH3OH(g),但目标方程式未出现CH3OH(g),可得出第三个方程式用不到,根据观察发现,②-①可以得到![]() ,
,![]() 用盖斯定律计算即可;
用盖斯定律计算即可;
(3)![]() 是一个气体体积不变的反应,故气体总物质的量=2mol+2mol=4mol,0-5分钟,CO含量减小了0.4,即减小了4×0.4mol=1.6mol,结合体积可计算浓度变化量,进而计算CO表示的速率,进而计算v[H2O(g)]。6分钟到9分钟,CO的含量下降,说明平衡正向移动,且6到9分钟CO含量减少程度比2到5分钟小,说明6分钟改变的条件使反应速率减小了;
是一个气体体积不变的反应,故气体总物质的量=2mol+2mol=4mol,0-5分钟,CO含量减小了0.4,即减小了4×0.4mol=1.6mol,结合体积可计算浓度变化量,进而计算CO表示的速率,进而计算v[H2O(g)]。6分钟到9分钟,CO的含量下降,说明平衡正向移动,且6到9分钟CO含量减少程度比2到5分钟小,说明6分钟改变的条件使反应速率减小了;
(4)①分析图发现,低温时,无论压强多大,CO的转化率都相等;
②实际化工生产除了需要考虑平衡原理外,还要考虑实际生产效率、成本投入等。
(1)①恒温恒容下,增大氢气的起始量,压强增大,平衡正向移动,氢气的转化率增大,结合图像可知:n1<n2<n3,故答案为:n1<n2<n3;
②该反应中只有氢气一种气体,则容器压强与氢气的物质的量成正比,温度T1时,起始时,压强为9kPa,平衡时,压强为3kPa,设平衡时氢气的物质的量为n,则![]() ,解得:n=
,解得:n=![]() ,则平衡时,c(H2)=
,则平衡时,c(H2)=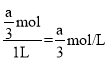 ,所以,K=
,所以,K= =
=![]() ,故答案为:
,故答案为:![]() ;
;
③假设平衡不移动,则t6时刻将容积压缩至原容积的一半,压强应变为t6时刻压强的2倍,即6kPa,但实际情况是,平衡正向移动,气体分子数减小,所以,此时容器内的压强小于6kPa,故答案为:小于;
(2)②-①得:![]() =(-41kJ·mol-1)-(+165kJ·mol-1)=-206 kJ·mol-1,故答案为:-206 kJ·mol-1;
=(-41kJ·mol-1)-(+165kJ·mol-1)=-206 kJ·mol-1,故答案为:-206 kJ·mol-1;
(3)![]() 是一个气体分子总数不变的反应,故气体总物质的量=2mol+2mol=4mol,0-5分钟,CO含量减小了0.4,即减小了4×0.4mol=1.6mol,则CO浓度减小了
是一个气体分子总数不变的反应,故气体总物质的量=2mol+2mol=4mol,0-5分钟,CO含量减小了0.4,即减小了4×0.4mol=1.6mol,则CO浓度减小了![]() =0.16mol/L,v(CO)=
=0.16mol/L,v(CO)=![]() =0.032mol/L,由方程式计量数可知v[H2O(g)]=v(CO)= 0.032mol/L。由分析可知,6分钟时改变的条件使平衡正向移动、同时反应速率减小,又从表格可知,6分钟时CO含量没有变化,不可能是移走生成物,综上所述,6分钟时,降低了温度,故答案为:0.032mol/L;降低温度;
=0.032mol/L,由方程式计量数可知v[H2O(g)]=v(CO)= 0.032mol/L。由分析可知,6分钟时改变的条件使平衡正向移动、同时反应速率减小,又从表格可知,6分钟时CO含量没有变化,不可能是移走生成物,综上所述,6分钟时,降低了温度,故答案为:0.032mol/L;降低温度;
(4)①由图可知,低温时,无论压强多大,CO的转化率几乎相等,则低温时,对CO转化率影响的主要因素是温度,故答案为:温度;
②温度太低,反应速率太慢,不利于甲醇的合成,压强太大,设备抗压要求增大,设备成本增加,故实际生产往往采用300~400 °C和10 MPa的条件,故答案为:温度太低,反应速率太慢,不利于甲醇的合成,压强太大,设备要求提高,成本增加。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案