题目内容
【题目】2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家。有两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂为正极的磷酸铁锂电池。请回答下列问题:
(1)基态钴原子的价电子排布式为____,Mn位于元素周期表的____ 区(填“s”或“p”或“d”或“ds”或“f”)。
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是___。PO43-的空间构型是 ___,中心原子的杂化方式是 ____。
(3)CoO、MnO两种氧化物的熔点由高到低的顺序是 ___,原因是 ___。
(4)PH3是____分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是 _____
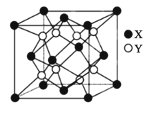
(5)硫化锂Li2S(摩尔质量Mgmol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ag.cm-3,则距离最近的两个S2-的距离是___nm。(用含a、M、NA的计算式表示)
【答案】3d74s2 d HPO3 正四面体 sp3 CoO>MnO CoO和MnO都属于离子晶体,离子半径:r(Mn2+)>r(Co2+),CoO的晶格能大于MnO的晶格能 极性 NH3能与水分子形成氢键,而PH3不能,所以在水中的溶解性PH3小 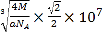
【解析】
(1)钴(Co)的核电荷数为27,基态钴原子的价电子排布式为为3d74s2,Mn位于元素周期表的第四周期第ⅦB族,属于d区,故答案为:3d74s2;d。
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,偏磷酸的酸性最强,次,亚,正依次减弱,PO43-的中P原子的价层电子对数为4,且不含孤对电子,所以空间构型是正四面体,中心原子的杂化方式是sp3,故答案为:HPO3;正四面体;sp3。
(3)CoO和MnO都属于离子晶体,离子半径:r(Mn2+)>r(Co2+),CoO的晶格能大于MnO的晶格能,熔点:CoO>MnO,故答案为:
CoO>MnO;CoO和MnO都属于离子晶体,离子半径:r(Mn2+)>r(Co2+),CoO的晶格能大于MnO的晶格能。
(4)PH3分子中磷原子形成了3个σ键,1个孤电子对,其价层电子对的总数是4,空间结构为三角锥形,是极性分子,NH3能与水分子形成氢键,所以在水中的溶解性NH3大于PH3,故答案为:极性;NH3能与水分子形成氢键,而PH3不能,所以在水中的溶解性PH3小。
(5)由晶胞结构可知,X原子个数为:![]() ,Y原子个数为:8,所以X为S2-,Y为Li+, 设晶胞的边长为bcm,
,Y原子个数为:8,所以X为S2-,Y为Li+, 设晶胞的边长为bcm,![]() ,
,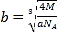 cm,距离最近的两个S2-的是面对角线的一般,面对角线为
cm,距离最近的两个S2-的是面对角线的一般,面对角线为![]() ,则距离最近的两个S2-的距离为
,则距离最近的两个S2-的距离为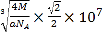 nm,故答案为:
nm,故答案为: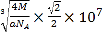 。
。