题目内容
【题目】如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分:
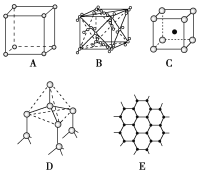
请回答下列问题:
(1)代表金刚石的是________(填编号字母,下同),其中每个碳原子与________个碳原子最接近且距离相等。金刚石属于________晶体。
(2)代表石墨的是________,每个正六边形占有的碳原子数平均为________个。
(3)代表NaCl的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(4)代表CsCl的是________,它属于________晶体,每个Cs+与________个Cl-紧邻。
(5)代表干冰的是________,它属于________晶体,每个CO2分子与________个CO2分子紧邻。
【答案】D 4 原子 E 2 A 12 C 离子 8 B 分子 12
【解析】
根据不同物质晶体的结构特点来辨别图形所代表的物质。NaCl晶胞是简单的立方单元,干冰也是立方体结构,但在立方体每个正方形面的中央都有一个CO2分子,称为“面心立方”,金刚石的基本单元是正四面体,为空间网状结构,石墨是分层结构。
(1)在金刚石晶胞中,每个碳原子可与周围4个碳原子形成共价键,将这4个碳原子连接起来后可以形成正四面体,体心是1个碳原子,所以图D为金刚石,每个碳原子与4个碳原子最近且距离相等,金刚石是空间网状结构,属于原子晶体,故答案为:D,4,原子。
(2)石墨是平面层状结构,在层与层之间以范德华力相互结合,在层内碳与碳以共价键相互作用,形成六边形,所以图E为石墨的结构,每个碳原子紧邻另外3个碳原子,即每个六边形占有1个碳原子的1/3,所以大的结构中每个六边形占有的碳原子数是6×1/3=2个,故答案为:E,2。
(3)在氯化钠晶胞中,每个Na+周围有6个Cl-,每个Cl-周围也有6个Na+,所以图A为氯化钠的结构,根据晶胞的结构,每个钠离子周围距离最近的钠离子在小立方体的面对角线的位置,每个钠离子周围有8个这样的立方体,所以每个钠离子周围与它最近且距离相等的钠离子就有12个,故答案为:A,12。
(4)CsCl的晶胞中铯离子与氯离子的配位数都是8,即每个铯离子周围有8个氯离子,每个氯离子周围有8个铯离子,所以,图C为CsCl的结构,属于离子晶体,故答案为:C,离子,8。
(5)干冰也是分子晶体,CO2位于立方体的面心和顶点上,以顶点上的CO2分子为例,与它距离最近的CO2分子分布在于该顶点相连的12个面的面心上,所以图B为干冰晶体,故答案为:B,分子,12。

【题目】在容积为1L的密闭容器中,发生反应N2+3H2![]() 2NH3△H<0,投入1molN2和3molH2分别在以下不同实验条件下进行反应。下列分析正确的是( )
2NH3△H<0,投入1molN2和3molH2分别在以下不同实验条件下进行反应。下列分析正确的是( )
容器编号 | 实验条件 | 平衡时反应中的能量变化 |
I | 恒温恒容 | 放热Q1kJ |
II | 恒温恒压 | 放热Q2kJ |
Ⅲ | 恒容绝热 | 放热Q3kJ |
A.放出热量:Q1>Q2
B.N2的转化率:I>Ⅲ
C.平衡时H2的浓度:I>Ⅲ
D.平衡时氨气的体积分数:I>II
【题目】氨气是一种重要的化工原料,在工农业中都有广泛的应用。
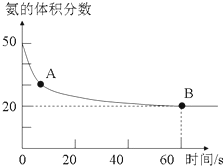
(1)NH3和CO2在120℃和催化剂的作用下可以合成尿素,反应方程式为2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)。某实验小组向一个容积不变的真空密闭容器中充入CO2与NH3合成尿素,在恒定温度下,混合气体中NH3的体积分数随时间的变化关系如图所示(该条件下尿素为固体)。A点的正反应速率v正(CO2)___ (填“大于”“小于”或“等于”)B点的逆反应速率v逆(CO2),NH3的平衡转化率为__。
CO(NH2)2(s)+H2O(g)。某实验小组向一个容积不变的真空密闭容器中充入CO2与NH3合成尿素,在恒定温度下,混合气体中NH3的体积分数随时间的变化关系如图所示(该条件下尿素为固体)。A点的正反应速率v正(CO2)___ (填“大于”“小于”或“等于”)B点的逆反应速率v逆(CO2),NH3的平衡转化率为__。
(2)氨基甲酸铵(NH2COONH4)是合成尿素过程的中间产物,现 将体积比为2∶1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:2NH3(g)+CO2(g)![]() NH2COONH4(s)。实验测得在不同温度下的平衡数据如下表:
NH2COONH4(s)。实验测得在不同温度下的平衡数据如下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡气体总浓度 (10-3mol·L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.6 |
①上述反应的焓变:ΔH__0,熵变ΔS__0(填“>”“<”或“=”)。
②下列说法能说明上述反应建立化学平衡状态的是_______。
A.混合气体的平均相对分子质量不再发生变化
B.混合气体中NH3与CO2的浓度之比不再发生变化
C.混合气体的密度不再发生变化 D.v正(NH3)=2v逆(CO2)
③根据表中数据,列出25.0℃时该反应的化学平衡常数的计算式K=_____(不要求计算结果),该反应温度每升高10℃,化学平衡常数就变为原来的______倍。