��Ŀ����
����Ŀ��FeCl3��һ�ֺ���Ҫ�����Σ���Ҫ������ˮ����������Ч���á��۸���˵��ŵ㣮��ҵ�Ͽɽ��������������У�������FeCl2 �� ��ͨ��Cl2�������Ʊ�FeCl3��Һ��
��֪���ٱ�״���£�1���ˮ��������ܽ�500�����HCl���ڱ���NaCl��Һ��Ũ��ԼΪ5.00molL��1 ��
��1���ڱ�״���£���44.8LHCl��������100mLˮ�У�������ҺA���ܶ�Ϊ1.038gcm��3 �� ����Һ��HCl�����ʵ���Ũ��Ϊ������ʹ����NaCl��Һ��Cl��Ũ������ҺA�е�Cl��Ũ����ȣ���Ӧ�ܽ�ԼL��״��HCl���壨��Һ����仯���Բ��ƣ���
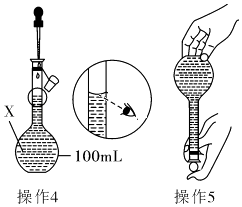
��2����ʵ������0.5molL��1NaCl��Һ240mL����Ӧ��ȡ�����mL�ı���NaCl��Һ�����ƣ������ƹ���
�У�ʹ��ǰ�������Ƿ�©Һ�����������������Ʋ���������ҺŨ��ƫ�ߵ�����ѡ���ţ���
A����ȡ��Һʱ������Һ�彦��
B������ƿ������ˮϴ�Ӹɾ���δ����
C������ʱ������Һ���ˮ���̶���
D��ת��Һ���δ������ˮϴ���ձ��Ͳ�����
E������Ͳ��ȡ��Һʱ���Ӷ���
F������ʱ�����������ߣ������ý�ͷ�ι��������ಿ��
��3��FeCl3��Һ����������ˮ���侻ˮ��ԭ��Ϊ�������ӷ���ʽ��ʾ������100mL��1molL��1��FeCl3��Һ��ˮʱ�����ɾ��о�ˮ���õ�����0.1NA������ڡ��������ڡ���С�ڡ�����
���𰸡�
��1��12mol/L��291.2
��2��25������ƿ��CE
��3��FeCl3+3H2O?Fe��OH��3�����壩+3HCl��С��
���������⣺��1������£�44.8L HCl�����ʵ���n= ![]() =
= ![]() =2mol��HCl������=2mol��36.5g/mol=73g��100mLˮ������ԼΪ100g����������Һ������Ϊ173g��������Һ�����Ϊ��V=
=2mol��HCl������=2mol��36.5g/mol=73g��100mLˮ������ԼΪ100g����������Һ������Ϊ173g��������Һ�����Ϊ��V= ![]() =
= ![]() mL��������Һ�����ʵ���Ũ��Ϊc=
mL��������Һ�����ʵ���Ũ��Ϊc= ![]() =
= ![]() =12mol/L������NaCl��Һ��Ũ��ԼΪ5.00molL��1 �� �����ܽ���Ȼ������Ϊ��12��5��mol/L��22.4L/mol=291.2L�����Դ��ǣ�12mol/L��291.2����2��������Һ240mL��Ҫѡ��250mL����ƿ��ϡ��ҺΪ0.5molL��1NaCl��Һ������NaCl��Һ��Ũ��ԼΪ5.00molL��1 �� n=cŨVŨ=cϡVϡ �� VŨ=
=12mol/L������NaCl��Һ��Ũ��ԼΪ5.00molL��1 �� �����ܽ���Ȼ������Ϊ��12��5��mol/L��22.4L/mol=291.2L�����Դ��ǣ�12mol/L��291.2����2��������Һ240mL��Ҫѡ��250mL����ƿ��ϡ��ҺΪ0.5molL��1NaCl��Һ������NaCl��Һ��Ũ��ԼΪ5.00molL��1 �� n=cŨVŨ=cϡVϡ �� VŨ= ![]() =25mL������ƿ������ʢ��Һ�壬���л�����ʹ��ʱ�������Ƿ�©ˮ��
=25mL������ƿ������ʢ��Һ�壬���л�����ʹ��ʱ�������Ƿ�©ˮ��
A����ȡ��Һʱ������Һ�彦�����������Ƶ���Һ�����ʵ����ʵ�����С�����Ƶ���ҺŨ��ƫ�ͣ���A����
B������ƿ������ˮϴ�Ӹɾ���δ��������ʵ����ʵ�������Һ��������������Ӱ�죬��������Һ��Ũ����Ӱ�죬��B����
C������ʱ������Һ���ˮ���̶��ߣ�������Һ�����ƫС����Һ��Ũ��ƫ�ߣ���C��ȷ��
D��ת��Һ���δ������ˮϴ���ձ��Ͳ��������������Ƶ���Һ�����ʵ����ʵ�����С�����Ƶ���ҺŨ��ƫ�ͣ���D����
E������Ͳ��ȡ��Һʱ���Ӷ������������Ƶ���Һ�����ʵ����ʵ���ƫ�����Ƶ���ҺŨ��ƫ�ߣ���E��ȷ��
F������ʱ�����������ߣ������ý�ͷ�ι��������ಿ�֣��������Ƶ���Һ�����ʵ����ʵ�����С�����Ƶ���ҺŨ��ƫ�ͣ���F����
���Դ��ǣ�25������ƿ��CE����3��FeCl3ˮ������Fe��OH��3���壬ˮ�ⷽ��ʽΪFeCl3+3H2OFe��OH��3�����壩+3HCl Na2CO3+H2O=NaHCO3+NaOH������������ˮ�е����������ˮ����Ϊˮ��Ϊ���淴Ӧ�������ɽ���Ϊ�����ӵļ����壬�����ɾ��о�ˮ���õ�����С��0.1NA ��
���Դ��ǣ�FeCl3+3H2OFe��OH��3�����壩+3HCl��С�ڣ�

����Ŀ����������ɸ�������ɺ����ʽ��з��ࣺ
��1��Na��K��H��O��C��S��N�������ֻ�����Ԫ����ɺ��ʵ����ʣ�����ѧʽ�ֱ����ڱ��ڵĺ��棻��ֻ����һ�֣�
������� | �� | �� | �� | ������ | �⻯�� |
��ѧʽ | ��H2SO4 | ��NaOH | ��Na2SO4 | ��SO2 | ��NH3 |
��2��д����ת��Ϊ��Ļ�ѧ����ʽ��
��3��д��Cu�͢ٵ�Ũ��Һ��Ӧ�Ļ�ѧ����ʽ��
��4��ʵ�����Ʊ��᳣������Ӧ�����������ķ����� ��