题目内容
【题目】A、B、C、D是四种常见的单质,A、B为金属,C、D常温下是气体,且D为黄绿色气体。甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质。它们之间的转化关系如下图所示:

请回答下列问题:
(1)B与甲反应的化学方程式是__________________________,该反应中如得到1molA则反应中转移的电子为_________ mol。
(2)常温下,将A或B的单质放入浓硫酸或浓硝酸中,是否溶解?___________(填“是”或“否”)。
(3)将丙溶于水配成溶液,检验丙中阳离子的方法是______________________。
(4)写出A与水蒸气反应生成C和甲的化学方程式____________________。
(5)将A、B两种金属按一定的质量比组成混合物。取一定质量的该混合物,向其中加入足量的NaOH溶液,生成气体的体积在标准状况下为n L,B与NaOH溶液反应的离子方程式是______________,混合物中B的物质的量为______________mol(用含字母的分数式表示)。、
【答案】![]()
![]() 否 取少量溶液于试管中,向试管中加入适量KSCN溶液,若溶液呈血红色,则证明溶液中含有Fe3+
否 取少量溶液于试管中,向试管中加入适量KSCN溶液,若溶液呈血红色,则证明溶液中含有Fe3+ ![]()
![]()
![]()
【解析】
A、B为金属,C、D常温下是气体,且D为黄绿色气体.甲、乙、丙为常见的化合物,甲是黑色且具有磁性的物质,结合转化关系可知,甲为四氧化三铁,B为Al,A为Fe,C为氢气,乙为偏铝酸钠,丙为氯化铁,然后结合元素化合物知识及化学用语来解答。
(1)Al与Fe3O4反应的方程式为:![]() ,Al元素化合价从0升高至+3价,每生成4molAl2O3,转移24mol电子,因此每生成1molFe,转移
,Al元素化合价从0升高至+3价,每生成4molAl2O3,转移24mol电子,因此每生成1molFe,转移![]() mol电子,
mol电子,
故答案为:![]() ;
;![]() ;
;
(2)常温下,Al、Fe与浓硫酸、浓硝酸反应会生成致密的氧化膜,而形成“钝化”,阻止反应的进一步进行,固体不能完全溶解,
故答案为:否;
(3)检验氯化铁溶液中Fe3+的常见方法:取少量溶液于试管中,向试管中加入适量KSCN溶液,若溶液呈血红色,则证明溶液中含有Fe3+,
故答案为:取少量溶液于试管中,向试管中加入适量KSCN溶液,若溶液呈血红色,则证明溶液中含有Fe3+;
(4)Fe与水蒸气反应生成Fe3O4和H2,其化学方程式为:![]() ,
,
故答案为:![]() ;
;
(5)Al与NaOH溶液反应的离子方程式为:![]() ,生成气体的体积在标准状况下体积为nL,n(H2)=
,生成气体的体积在标准状况下体积为nL,n(H2)=![]() mol,则n(Al)=
mol,则n(Al)=![]() mol×
mol×![]() =
=![]() mol,
mol,
故答案为:![]() ;
;![]() 。
。

【题目】实验室以苯甲醛为原料制备间溴苯甲醛的反应如下:
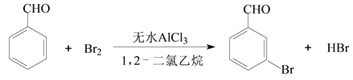
已知:①间溴苯甲醛温度过高时易被氧化。②溴、苯甲醛、1,2-二氯乙烷、间溴苯甲醛的沸点及相对分子质量见下表:
物质 | 溴 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 |
沸点/℃ | 58.8 | 179 | 83.5 | 229 |
相对分子质量 | 160 | 106 | 185 |
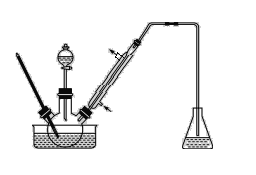
步骤1:将一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后装入三颈烧瓶(如图所示),缓慢滴加经浓硫酸干燥过的足量液溴,控温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机层用10% NaHCO3溶液洗涤。
步骤3:经洗涤的有机层加入适量无水MgSO4固体,放置一段时间后过滤出MgSO4nH2O晶体。
步骤4:分离有机层,收集相应馏分。
(1)实验装置中盛装液溴的仪器名称是_____,锥形瓶中的试剂为NaOH溶液其作用为________。
(2)步骤1反应过程中,为提高原料利用率,适宜的温度范围为(填序号)___。
A.>229℃ B.58.8℃~179℃ C.<58.8℃
(3)步骤2中用10% NaHCO3溶液洗涤,是为了除去溶于有机层的___(填化学式)。
(4)步骤4中采用何种蒸馏方式_______,其目的是为了防止________。
(5)若实验中加入了5.3 g苯甲醛,得到3.7 g间溴苯甲醛。则间溴苯甲醛产率为______。
【题目】有甲、乙两种物质:

(1)乙中含有的官能团的名称为:氯原子和______________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
![]()
其中反应I的反应类型是___________,反应II的条件是_______________,反应III的化学方程式为__________________________________(不需注明反应条件)。
(3)下列物质不能与乙反应的是_________(选填序号)。
a.金属钠 b.溴水 c.碳酸钠溶液 d.氢氧化钠溶液
(4)请设计实验证明乙中含有氯元素。
操作 | 现象 | 结论 |
______________ | ___________ | 乙中含有氯元素 |
【题目】四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如下表:
化学式 | SnCl2 | SnCl4 |
熔点/℃ | 246 | -33 |
沸点/℃ | 652 | 144 |
其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
回答下列问题:
(1)甲装置中仪器A的名称为___________。
(2)用甲装置制氯气,MnO4- 被还原为Mn2+,该反应的离子方程式为________________。
(3)将装置如图连接好,检查气密性,慢慢滴入浓盐酸,待观察到__________(填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:
①促进氯气与锡反应;
②_______________________________。
(4)如果缺少乙装置,可能发生的副反应的化学方程式为___________________;己装置的作用是_________________:
A.除去未反应的氯气,防止污染空气
B.防止空气中CO2气体进入戊装置
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2 的有_______________(填标号)。
A. H2O2溶液 B. FeCl3溶液(滴有KSCN) C. AgNO3溶液 D. 溴水
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为________。(保留3位有效数字)