题目内容
已知常温常压下, N≡N键的键能是946 KJ/mol 、N-H键的键能是391 KJ/mol、H-H 键的键能是436KJ/mol 。现有甲、乙两个容积相同的定容密闭容器,在常温下:①向密闭容器甲中通入1 mol N2和3 mol H2,达到平衡时放出热量Q1 kJ。②向密闭容器乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2 kJ。则下列关系式正确的是( )
| A.92>Ql>2Q2 | B.92=Q1<2Q2 | C.Q1=2Q2=92 | D.Q1=2Q2<92 |
A
试题分析:△H=
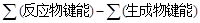 。N2(g)+3H2(g)
。N2(g)+3H2(g)  2NH3(g) △H=(946+3×436-391×6)kJ/mol=-92kJ/mol。可逆反应不能进行到底,1 mol N2和3 mol H2反应达到平衡时放出热量Q1<92kJ。容器乙中起始投料是容器甲中起始投料量的一半,容器乙相当于容器甲压强减小一半,平衡向左移动,所以2Q2<Q1。
2NH3(g) △H=(946+3×436-391×6)kJ/mol=-92kJ/mol。可逆反应不能进行到底,1 mol N2和3 mol H2反应达到平衡时放出热量Q1<92kJ。容器乙中起始投料是容器甲中起始投料量的一半,容器乙相当于容器甲压强减小一半,平衡向左移动,所以2Q2<Q1。点评:△H=
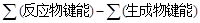 ;可逆反应不能进行到底。
;可逆反应不能进行到底。
练习册系列答案
相关题目
 2SO3(g),2min末测得容器中有7.2mol SO2。试回答:
2SO3(g),2min末测得容器中有7.2mol SO2。试回答: B(g)+D(g)在3种不同条件下进行,B和D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在3种不同条件下进行,B和D的起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表: 2HI(g)达到平衡状态的是 ( )
2HI(g)达到平衡状态的是 ( ) CO(g)+H2O(g)
CO(g)+H2O(g)

 CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 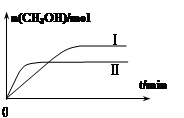
 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表: 2NO(g)达到平衡时NO的浓度 。(此温度下不考虑O2与NO的反应,计算结果保留两位有效数字)
2NO(g)达到平衡时NO的浓度 。(此温度下不考虑O2与NO的反应,计算结果保留两位有效数字) 4HCl+Si
4HCl+Si xC(g) + yD(g) (x、y为正整数),反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/(L·min),D的平衡浓度为0.3mol/L,又知v(B) : v(C)="3" : 2,则下列说法中正确的是
xC(g) + yD(g) (x、y为正整数),反应进行2min后达到平衡,这2min内平均反应速率v(C)=0.3mol/(L·min),D的平衡浓度为0.3mol/L,又知v(B) : v(C)="3" : 2,则下列说法中正确的是