题目内容
10.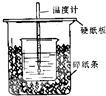 用50mL0.50mol/L盐酸与50mL0.55mol/L氢氧化钠溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/L氢氧化钠溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
(2)烧杯间填满碎纸条的作用是减少实验过程中的热量损失.
(3)大烧杯上如不盖硬纸板,求得的中和热数值偏小(填“偏大”、“偏小”或“无影响”).
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/L氢氧化钠溶液进行反应,与上述实验相比,所放出的热量不相等(填“相等”或“不相等”),简述理由反应放出的热量与酸碱的用量有关.
(5)用相同浓度和体积的氨水代替氢氧化钠溶液进行上述实验,测得的中和热的数值会偏小(填“偏大”、“偏小”或“无影响”).
分析 (1)根据量热计的构造来判断该装置的缺少仪器;
(2)中和热测定实验成败的关键是保温工作;
(3)不盖硬纸板,会有一部分热量散失;
(4)反应放出的热量和所用酸以及碱的量的多少有关;
(5)NH3•H2O是弱电解质,电离吸热.
解答 解:(1)根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒,故答案为:环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故答案为:减少实验过程中的热量损失;
(3)大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,故答案为:偏小;
(4)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL0.50mol/L盐酸与50mL0.55mol/L氢氧化钠溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高;
故答案为:不相等;反应放出的热量与酸碱的用量有关;
(5)NH3•H2O是弱电解质,电离过程为吸热过程,所以用氨水代替稀氢氧化钠溶液反应,反应放出的热量偏小,故答案为:偏小.
点评 本题考查中和热的测定原理、装置以及误差分析,掌握测定原理是解决问题的关键,难度不大.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
1.1831年李比希提出了确定有机物中氢和碳的质量分数的方法,其基本原理是在高温下氧化有机物,其生成物质主要是( )
| A. | CO和H2O | B. | CO和H2 | C. | CO2和H2O | D. | CO2和H2 |
18.应用Na2CO3和NaHCO3的下列性质设计实验,不能够鉴别Na2CO3和NaHCO3固体的是( )
| A. | 水溶性 | B. | 热稳定性 | C. | 与酸反应 | D. | 焰色反应 |
5.试写出中学阶段常见的两种制取氧气的化学方程式:H2O2$\frac{\underline{\;MnO_2\;}}{\;}$H2O+O2↑;2Na2O2+2H2O=4NaOH+O2↑.
Ⅱ.实验室中通常用MnO2作催化剂分解过氧化氢,已知CuSO4溶液对过氧化氢的分解也具有催化作用,某实验兴趣小组同学猜想其他盐溶液也可能在这个反应中起同样的作用,于是他们做了以下探究.请你帮助他们完成实验报告:
(1)实验过程:在一支试管中加入5mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管.
实验现象:试管中有大量的气泡产生,带火星的木条复燃.
实验结论:FeCl3溶液可以催化分解H2O2.
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-.
你认为最不可能的是甲同学的猜想,理由是因过氧化氢溶液中自身有水,可见水不是催化剂.
(3)同学们对余下的两个猜想,用实验进行了探究,并记录如下,请你仔细分析后填表:
实验过程实验现象结论
Ⅱ.实验室中通常用MnO2作催化剂分解过氧化氢,已知CuSO4溶液对过氧化氢的分解也具有催化作用,某实验兴趣小组同学猜想其他盐溶液也可能在这个反应中起同样的作用,于是他们做了以下探究.请你帮助他们完成实验报告:
(1)实验过程:在一支试管中加入5mL 5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管.
实验现象:试管中有大量的气泡产生,带火星的木条复燃.
实验结论:FeCl3溶液可以催化分解H2O2.
(2)已知FeCl3在水中可解离出Fe3+和Cl-,同学们提出以下猜想:
甲同学的猜想:真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想:真正催化分解H2O2的是FeCl3溶液中的Cl-.
你认为最不可能的是甲同学的猜想,理由是因过氧化氢溶液中自身有水,可见水不是催化剂.
(3)同学们对余下的两个猜想,用实验进行了探究,并记录如下,请你仔细分析后填表:
实验过程实验现象结论
| 实验过程 | 实验现象 | 结论 |
| 向盛有5mL 5%的H2O2溶液的试管中滴入少量的 HCl,把带火星的木条伸入试管. | 无明显现象 | 起催化作用的 不是Cl- |
| 向盛有5mL 5%的H2O2溶液的试管中滴入少量的Fe2(SO4)3,把带火星的木条伸入试管. | 试管中有大量气泡产生,带火星的木条复燃. | 起催化作用的 是Fe3+ |
2.将amLNO、bmLNO2和cmLO2混合于同一试管中,将试管倒置于水中,充分反应后,试管内气体全部消失,则a:b:c不可能是( )
| A. | 1:1:1 | B. | 2:1:1 | C. | 3:7:4 | D. | 1:5:2 |
19.表中列出了前20号元素中的某些元素性质的有关数据:
试回答下列问题:
(1)以上10种元素的原子中,最容易失去电子的是②(填写编号);与H2最容易化合的非金属单质是氟气(写物质名称).
(2)写出元素⑤的氢化物结构式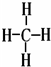 ;③和⑤形成的化合物的电子式
;③和⑤形成的化合物的电子式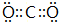 ;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式
;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式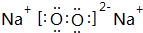 ;
;
(3)某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期第ⅥA族,请画出它的阴离子结构示意图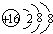 ,比较R的阴离子与②的阳离子半径大小(写离子符号)S2->K+
,比较R的阴离子与②的阳离子半径大小(写离子符号)S2->K+
(4)写出上述⑥、⑦两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式PCl3.
(5)写出④的最高价氧化物的水化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式3H++Al(OH)3=Al3++3H2O;OH-+Al(OH)3=AlO2-+2H2O.
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.52 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | - |
| 最低价态 | - | - | -2 | - | -4 | -3 | -1 | - | -3 | -1 |
(1)以上10种元素的原子中,最容易失去电子的是②(填写编号);与H2最容易化合的非金属单质是氟气(写物质名称).
(2)写出元素⑤的氢化物结构式
 ;③和⑤形成的化合物的电子式
;③和⑤形成的化合物的电子式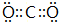 ;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式
;写出元素③和⑧形成的既有离子键,又有共价键的化合物的电子式 ;
;(3)某元素R的原子半径为1.02×10-10m,该元素在周期表中位于第三周期第ⅥA族,请画出它的阴离子结构示意图
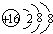 ,比较R的阴离子与②的阳离子半径大小(写离子符号)S2->K+
,比较R的阴离子与②的阳离子半径大小(写离子符号)S2->K+(4)写出上述⑥、⑦两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的一种物质的分子式PCl3.
(5)写出④的最高价氧化物的水化物分别跟⑦和⑧的最高价氧化物的水化物反应的离子方程式3H++Al(OH)3=Al3++3H2O;OH-+Al(OH)3=AlO2-+2H2O.
20.1.8g某金属与足量盐酸充分反应,产生2.24LH2(标况下),则该金属是( )
| A. | Zn | B. | Mg | C. | Al | D. | Fe |