��Ŀ����
����Ŀ�����п�ͼ�е���ĸ�ֱ����һ�ֳ��������ʻ�����Һ���֮���ת����ϵ����ͼ��ʾ�����ֲ��P��Ӧ��������ȥ������֪A��BΪ��̬���ʣ�F�ǵؿ��к������Ľ���Ԫ�صĵ��ʣ�E��H��IΪ�����EΪ��ɫ���壬IΪ����ɫ���壻MΪ���ɫ��������ش��������⣺
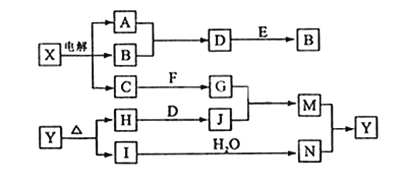
��1��B������Ԫ��λ�����ڱ��е�____����____�塣
��2��A��B��ȼ�յ�������_______________��
��3��D+E��B�ķ�Ӧ�У��������뱻��ԭ�����ʵ����ʵ�������________��
��4��G+J��M�����ӷ���ʽ�� _________________��
��5��Y���ȷֽ�Ļ�ѧ����ʽ�� ___________________��
���𰸡�����A������ɫ����2:13AlO2-+Fe3++6H2O��3Al��OH��3��+Fe��OH��3��4Fe��NO3��3![]() 2Fe2O3 +12NO2��+3O2��
2Fe2O3 +12NO2��+3O2��
��������
����A��BΪ��̬�����������ͼ����ʾ����Ϣ��A��B��C����X�����������²���÷�ӦΪ��ⱥ��ʳ��ˮ��Ӧ���ɵ�XΪNaCl��CΪNaOH��A��BΪH2��Cl2���������ĸ���Cl2��Ҫ���ݺ������Ϣ��֪����D��A��B��Ӧ�õ�����DΪHCl������EΪ��ɫ������Ϊ��������������ͼ����ʾ������B��D��HCl����E��Ӧ�õ������Ʋ���÷�ӦΪʵ�������ȷ�Ӧ����EΪMnO2��BΪCl2��AΪH2�����������F�ǵؿ��к������Ľ���Ԫ�صĵ������ɵã�FΪAl��G��C��NaOH����F��Al����Ӧ�ã���GӦΪNaAlO2�����������IΪ��������Ϊ����ɫ��������IΪNO2������MΪ���ɫ��������֪MΪFe(OH)3��ͬʱҲ˵��Y�д���Ԫ��Fe������HΪ���������Լ���IΪNO2���ɲ²��Y![]() H+I��ӦӦΪ�����ηֽⷴӦ��4Fe(NO3)3
H+I��ӦӦΪ�����ηֽⷴӦ��4Fe(NO3)3![]() 2Fe2O3��12NO2����3O2������YΪFe(NO3)3��HΪFe2O3��������JΪFeCl3��NΪHNO3���Ƴ�Ԫ�غ����δʹ�ù������������Ƿ���ȷ���Դ˽���С����
2Fe2O3��12NO2����3O2������YΪFe(NO3)3��HΪFe2O3��������JΪFeCl3��NΪHNO3���Ƴ�Ԫ�غ����δʹ�ù������������Ƿ���ȷ���Դ˽���С����
����A��BΪ��̬�����������ͼ����ʾ����Ϣ��A��B��C����X�����������²���÷�ӦΪ��ⱥ��ʳ��ˮ��Ӧ���ɵ�XΪNaCl��CΪNaOH��A��BΪH2��Cl2���������ĸ���Cl2��Ҫ���ݺ������Ϣ��֪����D��A��B��Ӧ�õ�����DΪHCl������EΪ��ɫ������Ϊ��������������ͼ����ʾ������B��D��HCl����E��Ӧ�õ������Ʋ���÷�ӦΪʵ�������ȷ�Ӧ����EΪMnO2��BΪCl2��AΪH2�����������F�ǵؿ��к������Ľ���Ԫ�صĵ������ɵã�FΪAl��G��C��NaOH����F��Al����Ӧ�ã���GӦΪNaAlO2�����������IΪ��������Ϊ����ɫ��������IΪNO2������MΪ���ɫ��������֪MΪFe(OH)3��ͬʱҲ˵��Y�д���Ԫ��Fe������HΪ���������Լ���IΪNO2���ɲ²��Y![]() H+I��ӦӦΪ�����ηֽⷴӦ��4Fe(NO3)3
H+I��ӦӦΪ�����ηֽⷴӦ��4Fe(NO3)3![]() 2Fe2O3��12NO2����3O2������YΪFe(NO3)3��HΪFe2O3��������JΪFeCl3��NΪHNO3��
2Fe2O3��12NO2����3O2������YΪFe(NO3)3��HΪFe2O3��������JΪFeCl3��NΪHNO3��
��1��BΪCl2��Clλ��Ԫ�����ڱ��е����������塣
��2������(A)������(B)��ȼ�յ������Dz�����ɫ���档
��3��D + E �� BΪʵ�������ȷ�Ӧ����ѧ����ʽΪ4HCl(Ũ)��MnO2![]() MnCl2 ��Cl2����2H2O���ɼ��������뱻��ԭ�����ʵ���֮��Ϊ2:1��
MnCl2 ��Cl2����2H2O���ɼ��������뱻��ԭ�����ʵ���֮��Ϊ2:1��
��4���÷�ӦΪ˫ˮ�ⷴӦ��3[Al(OH)4]����Fe3��===3Al(OH)3����Fe(OH)3����
��5����Ϊ�����β��ȶ����ȷֽⷴӦ��4Fe(NO3)3![]() 2Fe2O3��12NO2����3O2����
2Fe2O3��12NO2����3O2����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ���±�Ϊ���ڱ�ǰ20��Ԫ����ijЩԪ�ص��й����ݣ�
Ԫ������ | �� | �� | �� | �� | �� | �� | �� | �� | �� | �� |
ԭ�Ӱ뾶��10-10m�� | 1.86 | 1.52 | 0.66 | 0.53 | 0.77 | 1.10 | 0.99 | 2.31 | 0.70 | 0.64 |
���̬ | +1 | +1 | ���� | +1 | +4 | +5 | +7 | +1 | +5 | ���� |
��ͼ�̬ | ���� | ���� | ��2 | -1 | -4 | ��3 | ��1 | ���� | ��3 | ��1 |
�Իش��������⣺(�ö�Ӧ��Ԫ�ط��Ż����ʵĻ�ѧʽ��ʾ)
��1��д�����ԭ�ӽṹʾ��ͼ��________��
��2�������ݡ��ޡ��ߺ�Ԫ����ij2��Ԫ���γɵĻ������У�ÿһ��ԭ�Ӷ����������Ϊ8�����ȶ��ṹ�����ʿ�����______��____��
��3��ijԪ��R��ԭ�Ӱ뾶Ϊ1.04��10-10m����Ԫ�������ڱ��е�λ����___________��
��4������10��Ԫ�ص�ԭ���У���ԭ����ǿ����__________��Ԫ�ط��ţ���
��5���ۡ��ߡ��١�������Ԫ���γɵ����ӣ���뾶��С�����˳��Ϊ___________��
����Ŀ��N2O5��һ����������������һ���¶��¿ɷ������·�Ӧ��2N2O5(g)![]() 4NO2(g)+O2(g) ��H��0��T1�¶�ʱ�����ܱ�������ͨ��N2O5���壬����ʵ�����ݼ��±���
4NO2(g)+O2(g) ��H��0��T1�¶�ʱ�����ܱ�������ͨ��N2O5���壬����ʵ�����ݼ��±���
ʱ��/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/��mol��L��1�� | 5.00 | 3.52 | 2.50 | 2.50 |
����˵����ȷ����
A. 500s��O2��ƽ����������Ϊ7.4��l0��4mol��L��1��s��1
B. T1�¶��¸÷�Ӧ�ﵽƽ��ʱ��ƽ��������NO2���������Ϊ50%
C. �ﵽƽ��������������䣬���������ѹ����ԭ����1/2����c(N2O5)��5.00mol��L��1
D. T1�¶��µ�ƽ�ⳣ��ΪK1��T2�¶��µ�ƽ�ⳣ��ΪK2����K1��K2����T1��T2