题目内容
【题目】某小组为研究电化学原理,设计如图装置。下列叙述正确的是
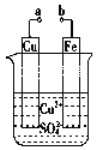
A. a和b不连接时,铁片上会发生氧化反应而质量减少
B. a和b用导线连接时,铜片上发生的反应为:Cu-2e-===Cu2+
C. 无论a和b是否连接,铁片均会被氧化,溶液均有Fe2+生成
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
【答案】C
【解析】A. a和b不连接时,铁片上会发生氧化反应但铁置换出铜而使铁的质量增大,选项A错误;B、a和b用导线连接时形成原电池,铜片为正极,发生的反应为: Cu2++2e-= Cu,选项B错误;C.根据选项A、B分析,无论a和b是否连接,铁片均会被氧化,溶液中均有Fe2+生成,选项C正确;D、a和b分别连接直流电源正、负极,电压足够大时,依据电解原理,阳离子移向阴极,所以Cu2+向铁电极移动,选项D错误。答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
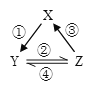
【题目】X、Y、Z 是中学化学中常见的三种物质,下表各组物质之间通过一步反应不能实现右图所示转化关系的是
X | Y | Z | 箭头上所标数字的反应条件 | ||
A. | NO | NO2 | HNO3 | ①常温遇氧气 |
|
B. | NaOH | Na2CO3 | NaHCO3 | ②通入适量CO2 | |
C. | Cu | CuSO4 | Cu(OH)2 | ③加热 | |
D. | Al2O3 | NaAlO2 | Al(OH)3 | ④加NaOH溶液 |
A. A B. B C. C D. D