题目内容
9.(1)Al2O3和Al(OH)3既可以与酸反应,又可以与碱反应,它们分别是两性氧化物和两性氢氧化物.(2)新制的氯水滴在蓝色石蕊试纸上现象蓝色石蕊试纸先变红色后褪色,说明氯水具有酸性和漂白性.
(3)碳酸氢钠的化学式是NaHCO3,俗称小苏打,其水溶液显碱性.(填“酸”、“碱”或“中”).
(4)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 (1)能和强酸、强碱反应的氧化物、氢氧化物分别是两性氧化物、两性氢氧化物;
(2)氯气和水反应生成HCl和HClO,两种酸电离出氢离子而导致氯水呈酸性,湿润的蓝色石蕊试纸遇酸变红色;HClO具有漂白性;
(3)碳酸氢钠俗称小苏打,碳酸氢钠中碳酸氢根离子水解程度大于电离程度导致溶液呈碱性;
(4)碳酸钠较稳定,加热条件下不易分解,碳酸氢钠不稳定,受热易分解生成碳酸钠.
解答 解:(1)能和强酸、强碱反应的氧化物、氢氧化物分别是两性氧化物、两性氢氧化物,Al2O3和Al(OH)3既可以与酸反应,又可以与碱反应,所以它们分别是两性氧化物和两性氢氧化物,故答案为:酸;碱;
(2)氯气和水反应生成HCl和HClO,两种酸电离出氢离子而导致氯水呈酸性,湿润的蓝色石蕊试纸遇酸变红色,所以新制氯水滴在蓝色石蕊试纸上先变红色;HClO具有漂白性,能使红色石蕊试纸漂白,所以看到的现象是:蓝色石蕊试纸先变红色后褪色,该现象说明氯水具有酸性和漂白性,
故答案为:蓝色石蕊试纸先变红色后褪色;酸;漂白;
(3)碳酸氢钠俗称小苏打,化学式为NaHCO3,碳酸氢钠中碳酸氢根离子水解程度大于电离程度导致溶液呈碱性,故答案为:NaHCO3;小苏打;碱;
(4)碳酸钠较稳定,加热条件下不易分解,碳酸氢钠不稳定,受热易分解生成碳酸钠,所以可以采用加热方法除去碳酸氢钠,反应方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 本题考查元素化合物知识,涉及除杂、盐类水解、次氯酸的漂白性、基本概念等知识点,明确物质性质是解本题关键,会根据物质性质选取合适的方法除杂,除杂时不能引进新的杂质.

| A. | $\frac{22.4m}{n}$ | B. | $\frac{22400m}{n}$ | C. | $\frac{22400n}{m}$ | D. | $\frac{n}{22.4m}$ |
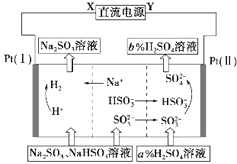 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中不正确的是( )| A. | X为直流电源的负极,Y为直流电源的正极 | |
| B. | 阳极区pH增大 | |
| C. | 阴极区的电极反应为:2H++2e=H2↑ | |
| D. | 该过程中可以循环利用的物质是Na2SO3 |
| A. | 15种 | B. | 28种 | C. | 32种 | D. | 40种 |
| A. | H2 | B. | N2 | C. | O2 | D. | Cl2 |
| A. | 13 | B. | 13 | C. | 11 | D. | 10 |
| A. | 1mol含8个碳原子的某烃分子,最多形成8mol碳碳单键 | |
| B. | 7.2 g 过氧化钙(CaO2)固体中阴、阳离子总数为0.2NA | |
| C. | 1 mol Cl2发生反应时,转移的电子数一定是2NA | |
| D. | 精炼铜过程中阳极减轻6.4g时,电路中转移电子数一定是0.2NA |
| A. | 向酒精灯内添加酒精时,不能多于容积的$\frac{2}{3}$,若不慎洒出的酒精在桌上燃烧,应迅速用水扑灭 | |
| B. | 中和滴定实验中,滴定管、锥形瓶用蒸馏水洗净后须再用待装液润洗后方可使用 | |
| C. | 取少量硫酸亚铁铵晶体放入试管,加入适量NaOH溶液,加热试管,在试管口用湿润的蓝色石蕊试纸检验,则可证明硫酸亚铁铵晶体的成分中含有NH4+ | |
| D. | 探究反应速率影响因素的实验中,以Na2S2O3溶液与稀硫酸反应产生沉淀的快慢为依据来比较不同条件下速率的快慢 |
| A. | 甲烷的燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 由N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol-1热化学方程式可知,当反应中转移6NA电子时,反应放出的热小于92.4 kJ | |
| C. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| D. | 在101 kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(1)△H=-571.6 kJ•mol-1 |