题目内容
13.(1)CH2=CH-CH2-Br中含有官能团的名称:溴原子、碳碳双键;(2)
 的系统命名:3,4-二甲基已烷;
的系统命名:3,4-二甲基已烷;(3)
 的键线式:
的键线式: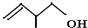 .
.
分析 (1)根据该有机物的结构简式写出其含有的官能团名称;
(2)该有机物为烷烃,根据烷烃的命名原则写出该有机物名称;
(3)根据有机物的结构简式及键线式的书写方法写出其键线式;
解答 解:(1)CH2=CH-CH2-Br中含有的官能团为溴原子和碳碳双键,
故答案为:溴原子、碳碳双键;
(2) ,该有机物最长碳链含有6个C,主链为己烷,编号从两边都可以,在3、4号C各含有1个甲基,该有机物名称为:3,4-二甲基已烷,
,该有机物最长碳链含有6个C,主链为己烷,编号从两边都可以,在3、4号C各含有1个甲基,该有机物名称为:3,4-二甲基已烷,
故答案为:3,4-二甲基已烷;
(3) 中含有官能团羟基和碳碳双键,改写成键线式为:
中含有官能团羟基和碳碳双键,改写成键线式为: ,
,
故答案为: ;
;
点评 本题考查了有机物命名、烃的衍生物官能团等知识,题目难度中等,注意掌握常见有机物的命名原则,明确常见有机反应方程式的书写方法,熟悉烃的衍生物的官能团结构及名称.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
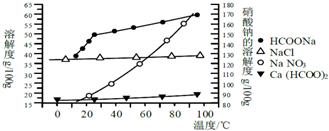
3.某研究性学习小组用工业碳酸钙(主要成分为CaCO3;杂质为:Al2O3、FeCO3) 为原料,先制备无机钙盐,再与甲酸钠溶液混合制取甲酸钙.结合如图几种物质的溶解度曲线及表中相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算),现提供的试剂有:
a.甲酸钠,b.5mol•L-1硝酸,c.5mol•L-1盐酸,d.5mol•L-1硫酸,e.3%H2O2溶液,f.澄清石灰水.
请补充完整由碳酸钙制备甲酸钙的实验步骤
步骤1.称取13.6g甲酸钠溶于约20mL水,配成溶液待用,并称取研细的碳酸钙样品10g待用.
步骤2.用稍过量硝酸溶解碳酸钙样品.
步骤3.用石灰水调整溶液pH=5.
步骤4.过滤后,将滤液与甲酸钠溶液混合,调整溶液pH 7~8,充分搅拌,所得溶液经蒸发浓缩(蒸发结晶)、趁热过滤、洗涤干燥得甲酸钙晶体.
a.甲酸钠,b.5mol•L-1硝酸,c.5mol•L-1盐酸,d.5mol•L-1硫酸,e.3%H2O2溶液,f.澄清石灰水.
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
步骤1.称取13.6g甲酸钠溶于约20mL水,配成溶液待用,并称取研细的碳酸钙样品10g待用.
步骤2.用稍过量硝酸溶解碳酸钙样品.
步骤3.用石灰水调整溶液pH=5.
步骤4.过滤后,将滤液与甲酸钠溶液混合,调整溶液pH 7~8,充分搅拌,所得溶液经蒸发浓缩(蒸发结晶)、趁热过滤、洗涤干燥得甲酸钙晶体.

4.下列是某同学对NaHSO4的物质类型进行的分析,其中不正确的是( )
| A. | 根据元素组成可判断是化合物 | |
| B. | 因它电离会生成钠离子又符合盐的组成,故可属于钠盐 | |
| C. | 因它电离会生成硫酸根离子又符合盐的组成,故可属于硫酸盐 | |
| D. | NaHSO4溶于水可电离出氢离子故可以称为酸 |
1.如表是不同温度下水的离子积数据:
试回答以下几个问题:
(1)若25<t1<t2,则a>1×10-14(填“<”、“>”或“=”);
(2)在25℃下,0.05mol/L的Ba(OH)2溶液的pH=13;
(3)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH-)为:1×10-10mol/L;
(4)在t2℃下,将pH=9的氢氧化钠溶液V1L与pH=4的硫酸溶液V2L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1:V2=$\frac{1}{9}$.
| 温度/℃ | 25 | t1 | t2 |
| Kw/mol2•L-2 | 1×10-14 | a | 1×10-12 |
(1)若25<t1<t2,则a>1×10-14(填“<”、“>”或“=”);
(2)在25℃下,0.05mol/L的Ba(OH)2溶液的pH=13;
(3)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH-)为:1×10-10mol/L;
(4)在t2℃下,将pH=9的氢氧化钠溶液V1L与pH=4的硫酸溶液V2L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1:V2=$\frac{1}{9}$.
8.反应C(s)+H2O(g)?CO(g)+H2(g)在一容积可变的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 保持体积不变,增加H2O(g)的物质的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 保持体积不变,充入N2使体系压强增大 | |
| D. | 保持压强不变,充入N2使容器体积变大 |
18.下列关于氧化性、还原性的判断正确的是( )
| A. | B的阳离子的氧化性比A的阳离子强,说明A元素的金属性一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2=2FeCl3+4FeI3 | |
| D. | 一定量氯气通入30 mL 10.00 mol•L-1的氢氧化钠溶液中,加热后形成NaCl、NaClO、NaClO3共存的溶液,若反应中转移的电子为n mol,则0.15<n<0.25 |
2.下列各项中表达正确的是( )
| A. | H、D、T表示同一种核素 | B. | F原子结构示意图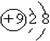 | ||
| C. | 用电子式表示HCl形成过程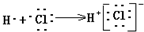 | D. | 羟基:-OH |
3.下列说法正确的是( )
| A. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| B. | CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| C. | 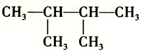 的名称是2,3-甲基丁烷 的名称是2,3-甲基丁烷 | |
| D. | 乙醇可与水以任意比例混溶,是因为与水形成了氢键 |
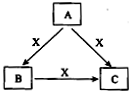 Ⅰ.A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示. 若A、B、C的焰色反应均呈黄色,水溶液均为碱性.
Ⅰ.A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图所示. 若A、B、C的焰色反应均呈黄色,水溶液均为碱性.