题目内容
【题目】某化学兴趣小组为探究元素性质的递变规律,设计可如下系列实验.
(1)①将钠、钾、镁、铝各1mol分别投入到足量的0.1molL﹣1的盐酸中,写出与盐酸反应最慢的金属发生反应的离子方程式 .
②将NaOH溶液与NH4Cl溶液混合生成NH3H2O,从而验证NaOH的碱性大于NH3H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由: .
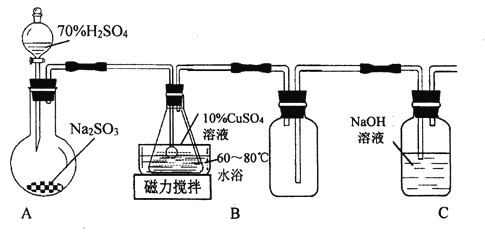
(2)利用如图装置可以验证非金属性的变化规律. 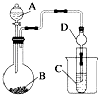
③实验室中提供药品Na2S,MnO2、浓盐酸、KMnO4 , 若要证明非金属性Cl>S;装置A,B,C中所装药品分别为 , 装置C中的实验现象为有淡黄色沉淀生成,离子方程式为 .
④若要证明非金属性:C>Si,则A中加、B中加Na2CO3、C中加Na2SiO3 , 则观察装置C中的实验现象为有白色沉淀生成.离子方程式为 . (假设所通气体是过量的).
【答案】
(1)2Al+6H+=2Al3++3H2↑;不合理,用碱性强弱比较金属性强弱时,一定要用元素最高价氧化物对应水化物的碱性强弱比较,NH3H2O不是N元素最高价氧化物对应的水化物
(2)浓盐酸、KMnO4、Na2S;S2﹣+Cl2=S↓+2Cl﹣;硫酸或H2SO4;SiO32﹣+2CO2+2H2O=H2SiO3↓+2HCO3﹣
【解析】解:(1)①同一周期元素,金属性随着原子序数增大而减弱,元素的金属性越强,同一主族,原子序数越大,金属性越强,其单质与酸或水反应越剧烈,所以金属性K>Na>Mg>Al,则K与盐酸反应最剧烈、Al与盐酸反应速率最慢,离子反应为:2Al+6H+=2Al3++3H2↑,故答案为:2Al+6H+=2Al3++3H2↑;②将NaOH溶液与NH4Cl溶液混合生成NH3H2O,可以说明NaOH的碱性大于NH3H2O,但不能说明Na的金属性大于N,因为要验证金属性的强弱,必须通过比较最高价氧化物所对应的水化物的碱性来进行比较,而NH3H2O不是氮元素的最高价氧化物的水化物,故答案为:不合理,用碱性强弱比较金属性强弱时,一定要用元素最高价氧化物对应水化物的碱性强弱比较,NH3H2O不是N元素最高价氧化物对应的水化物;(2)③设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证,则装置A、B、C中所装药品应分别为浓盐酸、KMnO4、Na2S溶液,装置C中的实验现象为有淡黄色沉淀生成,装置C中发生反应的离子方程式为S2﹣+Cl2═S↓+2Cl﹣ , 故答案为:浓盐酸、KMnO4、Na2S;S2﹣+Cl2═S↓+2Cl﹣;④若要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明,由于B中加Na2CO3 , 故A中可以加硫酸,通过硫酸和碳酸钠的反应来制取CO2 , 然后的CO2通入C中的Na2SiO3中,可以发生反应:Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3 , 离子反应为:SiO32﹣+2CO2+2H2O=H2SiO3↓+2HCO3﹣ , 产生白色胶状沉淀,从而可以证明酸性:H2CO3>H2SiO3 , 故非金属性:C>Si.故答案为:硫酸或H2SO4;SiO32﹣+2CO2+2H2O=H2SiO3↓+2HCO3﹣ .
(1)①元素的金属性越强,其单质与酸或水反应越剧烈;②元素的最高价氧化物的水化物的碱性越强,元素的金属性越强;(2)③设计实验验证非金属性:Cl>S,利用氯气与Na2S的氧化还原反应可验证;④要证明非金属性:C>Si,可以通过二氧化碳和硅酸钠反应生成难溶性的硅酸来证明.