ĢāÄæÄŚČŻ
”¾ĢāÄæ”æŌŚŅ»¶ØĢå»żµÄĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠČēĻĀ»Æѧ·“Ó¦£ŗ
CO£Øg£©+H2O£Øg£© ![]() CO2£Øg£©+H2£Øg£©£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKŗĶĪĀ¶ČtµÄ¹ŲĻµČē±ķ£ŗ
CO2£Øg£©+H2£Øg£©£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKŗĶĪĀ¶ČtµÄ¹ŲĻµČē±ķ£ŗ
t”ę | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ĪŖK= £¬ øĆ·“Ó¦ĪŖ·“Ó¦£ØŃ”Ģī”°ĪüČČ”±”¢”°·ÅČČ”±£©£®
£Ø2£©ÄÜÅŠ¶ĻøĆ·“Ó¦ŹĒ·ń“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ£»
A.ČŻĘ÷ÖŠŃ¹Ēæ²»±ä
B.»ģŗĻĘųĢåÖŠc£ØCO£©²»±ä
C.vÄę£ØH2£©=vÕż£ØH2O£©
D.c£ØCO2£©=c£ØCO£©
£Ø3£©830”ꏱ£¬ČŻĘ÷ÖŠµÄ·“Ó¦ŅŃ“ļµ½Ę½ŗā£®ŌŚĘäĖūĢõ¼ž²»±äµÄĒéæöĻĀ£¬ŌŚ“ĖĪĀ¶ČĻĀ£¬ČōøĆČŻĘ÷ÖŠŗ¬ÓŠ1molCO2”¢1.2molH2”¢0.75molCO”¢1.5molH2O£¬ÕāדĢ¬£ØŹĒ»ņ·ń£©“¦ÓŚĘ½ŗāדĢ¬£æČō²»ŹĒ£¬·“Ó¦ĻņÄÄøö·½Ļņ½ųŠŠ£æ £® £ØŃ”Ģī”°ĻņÕż·“Ó¦·½Ļņ”±”¢”°ĻņÄę·“Ó¦·½Ļņ”±£©£®
£Ø4£©Čō830”ꏱ£¬ĻņČŻĘ÷ÖŠ³äČėlmolCO”¢5molH2O£¬·“Ó¦“ļµ½Ę½ŗāŗó£¬COµÄ×Ŗ»ÆĀŹĪŖ £®
”¾“š°ø”æ
£Ø1£©![]() ,·ÅČČ
,·ÅČČ
£Ø2£©B,C
£Ø3£©·ń,ĻņÄę·“Ó¦·½Ļņ
£Ø4£©83.3%£Ø»ņ83%,»ņ5/6£©
”¾½āĪö”æ½ā£ŗ£Ø1£©»ÆŃ§Ę½ŗā³£ŹżKµČÓŚÉś³ÉĪļÅضČĆŻÖ®»żÓė·“Ó¦ĪļÅضČĆŻÖ®»żµÄ±Č£¬µ«²»°üŗ¬¹ĢĢåŗĶ“æŅŗĢ壬ĖłŅŌøĆ·“Ó¦»ÆŃ§Ę½ŗā³£ŹżK= ![]() £»ÉżøßĪĀ¶ČĘ½ŗāĻņĪüČČ·½ĻņŅĘ¶Æ£¬øł¾Ż±ķÖŠŹż¾ŻÖŖ£¬ÉżøßĪĀ¶Č»ÆŃ§Ę½ŗā³£Źż¼õŠ”£¬ĖµĆ÷Ę½ŗāÄęĻņŅĘ¶Æ£¬ŌņÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬
£»ÉżøßĪĀ¶ČĘ½ŗāĻņĪüČČ·½ĻņŅĘ¶Æ£¬øł¾Ż±ķÖŠŹż¾ŻÖŖ£¬ÉżøßĪĀ¶Č»ÆŃ§Ę½ŗā³£Źż¼õŠ”£¬ĖµĆ÷Ę½ŗāÄęĻņŅĘ¶Æ£¬ŌņÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬
ĖłŅŌ“š°øŹĒ£ŗ ![]() £»·ÅČČ£»
£»·ÅČČ£»
£Ø2£©A£®øĆ·“Ó¦Ē°ŗóĘųĢåĪļÖŹµÄĮæ²»±ä£¬ĖłŅŌ·“Ó¦ŹĒ·ń“ļµ½Ę½ŗāדĢ¬ČŻĘ÷ÖŠŃ¹Ē涼²»±ä£¬ĖłŅŌ²»ÄÜÅŠ¶ĻĘ½ŗāדĢ¬£¬¹Ź“ķĪó£»
B£®»ģŗĻĘųĢåÖŠc£ØCO£©²»±äŹ±£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹÕżČ·£»
C£®vÄę£ØH2£©=vÕż£ØH2O£©=vÕż£ØH2£©£¬ÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹ŹÕżČ·£»
D£®c£ØCO2£©=c£ØCO£©Ź±øĆ·“Ó¦æÉÄÜ“ļµ½Ę½ŗāדĢ¬Ņ²æÉÄÜƻӊ“ļµ½Ę½ŗāדĢ¬£¬Óė·“Ó¦Īļ³õŹ¼Įæ¼°×Ŗ»ÆĀŹÓŠ¹Ų£¬ĖłŅŌ²»ÄÜÅŠ¶ĻĘ½ŗāדĢ¬£¬¹Ź“ķĪó£»
¹ŹŃ”BC£»
£Ø3£©ŅņĪŖøĆ·“Ó¦ÖŠø÷ĘųĢå¼ĘĮæŹż¶¼ŹĒ1£¬ĖłŅŌ»ÆŃ§Ę½ŗā³£ŹżŅ²µČÓŚÉś³ÉĪļĪļÖŹµÄĮæÖ®»żÓė·“Ó¦ĪļĪļÖŹµÄĮæÖ®»żµÄ±Č£¬830”ꏱ£¬»ÆŃ§Ę½ŗā³£ŹżK=1.0£¬ČōøĆČŻĘ÷ÖŠŗ¬ÓŠ1molCO2”¢1.2molH2”¢0.75molCO”¢1.5molH2O£¬øĆĢåĻµÖŠÅضČÉĢ= ![]() =1.07£¾1£¬øĆ·“Ӧƻӊ“ļµ½Ę½ŗāדĢ¬£¬ŅŖŹ¹·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Ó¦øĆĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬
=1.07£¾1£¬øĆ·“Ӧƻӊ“ļµ½Ę½ŗāדĢ¬£¬ŅŖŹ¹·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Ó¦øĆĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬
ĖłŅŌ“š°øŹĒ£ŗ·ń£»ĻņÄę·“Ó¦·½Ļņ£»
£Ø4£©øĆĪĀ¶ČĻĀ»ÆŃ§Ę½ŗā³£ŹżKĪŖ1.0£¬Éč²Ī¼Ó·“Ó¦µÄn£ØCO£©=xmol£¬øł¾Ż·½³ĢŹ½ÖŖ£¬²Ī¼Ó·“Ó¦µÄn£ØH2O£©=n£ØH2£©=n£ØCO2£©=n£ØCO£©=xmol£¬K= ![]() £¬x=
£¬x= ![]()
×Ŗ»ÆĀŹ= ![]() ”Į100%=
”Į100%= ![]() =.83.3%£Ø»ņ83%£¬»ņ5/6£©£¬
=.83.3%£Ø»ņ83%£¬»ņ5/6£©£¬
ĖłŅŌ“š°øŹĒ£ŗ83.3%£Ø»ņ83%£¬»ņ5/6£©£®
”¾æ¼µć¾«Īö”æ½ā“š“ĖĢāµÄ¹Ų¼üŌŚÓŚĄķ½ā»ÆŃ§Ę½ŗāדĢ¬±¾ÖŹ¼°ĢŲÕ÷µÄĻą¹ŲÖŖŹ¶£¬ÕĘĪÕ»ÆŃ§Ę½ŗāדĢ¬µÄĢŲÕ÷£ŗ”°µČ”±¼“ VÕż=VÄę>0£»”°¶Æ”±¼“ŹĒ¶ÆĢ¬Ę½ŗā£¬Ę½ŗāŹ±·“Ó¦ČŌŌŚ½ųŠŠ£»”°¶Ø”±¼“·“Ó¦»ģŗĻĪļÖŠø÷×é·Ö°Ł·Öŗ¬Įæ²»±ä£»”°±ä”±¼“Ģõ¼žøÄ±ä£¬Ę½ŗā±»“ņĘĘ£¬²¢ŌŚŠĀµÄĢõ¼žĻĀ½ØĮ¢ŠĀµÄ»ÆŃ§Ę½ŗā£»ÓėĶ¾¾¶ĪŽ¹Ų£¬Ķā½ēĢõ¼ž²»±ä£¬æÉÄę·“Ó¦ĪŽĀŪŹĒ“ÓÕż·“Ó¦æŖŹ¼£¬»¹ŹĒ“ÓÄę·“Ó¦æŖŹ¼£¬¶¼æɽØĮ¢Ķ¬Ņ»Ę½ŗāדĢ¬£ØµČŠ§£©£¬ŅŌ¼°¶Ō»ÆŃ§Ę½ŗāµÄ¼ĘĖćµÄĄķ½ā£¬ĮĖ½ā·“Ó¦Īļ×Ŗ»ÆĀŹ=×Ŗ»ÆÅØ¶Č”ĀĘšŹ¼ÅØ¶Č”Į100%=×Ŗ»ÆĪļÖŹµÄĮæ”ĀĘšŹ¼ĪļÖŹµÄĮæ”Į100%£»²śĘ·µÄ²śĀŹ=Źµ¼ŹÉś³É²śĪļµÄĪļÖŹµÄĮæ”ĀĄķĀŪÉĻæɵƵ½²śĪļµÄĪļÖŹµÄĮæ”Į100%£®

 Š”Ģģ²ÅæĪŹ±×÷ŅµĻµĮŠ“š°ø
Š”Ģģ²ÅæĪŹ±×÷ŅµĻµĮŠ“š°ø Ņ»æĪĖÄĮ·ĻµĮŠ“š°ø
Ņ»æĪĖÄĮ·ĻµĮŠ“š°ø »ĘøŌŠ”דŌŖĀś·Ö³å“ĢĪ¢²āŃéĻµĮŠ“š°ø
»ĘøŌŠ”דŌŖĀś·Ö³å“ĢĪ¢²āŃéĻµĮŠ“š°ø ŠĀøؽĢµ¼Ń§ĻµĮŠ“š°ø
ŠĀøؽĢµ¼Ń§ĻµĮŠ“š°ø”¾ĢāÄæ”æĀČ»ÆŃĒķæ£ØSOCl2£©ŹĒŅ»ÖÖŅŗĢ¬»ÆŗĻĪļ£¬·ŠµćĪŖ 77”ę£¬ŌŚÅ©Ņ©”¢ÖĘŅ©ŠŠŅµÖŠÓĆĶ¾¹ć·ŗ”£SOCl2ÓöĖ®¾ēĮŅ·“Ó¦£¬ŅŗĆęÉĻ²śÉś°×Īķ£¬²¢“ųÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢå²śÉś£®ŹµŃéŹŅŗĻ³ÉŌĄķ£ŗSO2+Cl2+SCl2ØT2SOCl2£¬²æ·Ö×°ÖĆČēĶ¼ĖłŹ¾£¬(ŅŃÖŖ SCl2µÄ·ŠµćĪŖ 50”ę).
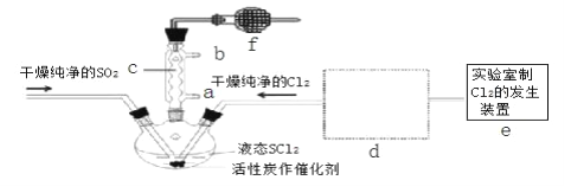
»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©ĻĀĮŠĖÄÖÖÖʱø SO2µÄ·½°øÖŠ×ī¼ŃŃ”ŌńŹĒ____________________________
·½°ø | A | B | C | D |
·¢Éś×°ÖĆ |
|
|
|
|
ĖłŃ”ŹŌ¼Į | 70%H2SO4+K2SO3 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | NaHCO3¹ĢĢå |
£Ø2£©ŅŌ MnO2ŗĶÅØŃĪĖįĪŖŌĮĻÖʱø Cl2µÄĄė×Ó·½³ĢŹ½ĪŖ___________________________
£Ø3£©ŅĒĘ÷ f µÄ×÷ÓĆŹĒ_________________________________________________
£Ø4£©d µÄŠéĻßæņÄŚŅžŗ¬Į½øö×°ÖĆ£¬°“ĘųĮ÷·½ĻņĖ³ŠņÕāĮ½øö×°ÖƵÄŅ©Ę··Ö±šŹĒ_______________”£
£Ø5£©ŹµŃé½įŹųŗó,½«Čż¾±ÉÕĘæ»ģŗĻĪļÖŠ²śĘ··ÖĄė³öĄ“µÄ·½·ØŹĒ _________________________
£Ø6£©ČōÓĆ SOCl2×÷ FeCl36H2O µÄĶŃĖ®¼Į£¬Éč¼ĘŹµŃéÖ¤Ć÷ĶŃĖ®Ź±·¢ÉśĮĖŃõ»Æ»¹Ō·“Ó¦”£Č”ÉŁĮæ FeCl36H2O ÓŚŹŌ¹ÜÖŠ£¬¼ÓČė¹żĮæ SOCl2£¬Õńµ“£¬ĶłŹŌ¹ÜÖŠ¼ÓĖ®Čܽā£¬µĪ¼Ó____________»ņ________ČÜŅŗ£¬Ö¤Ć÷ĶŃĖ®¹ż³Ģ·¢ÉśĮĖŃõ»Æ»¹Ō·“Ó¦”£