题目内容
12.除去下列溶液中的杂质(括号内是杂质),下列选项中所用试剂错误的是( )| A. | NaOH[Ba(OH)2]:使用Na2SO4溶液 | B. | KOH(K2SO4):使用Ba(OH)2溶液 | ||
| C. | NaCl(Na2SO4):使用Ba(NO3)2溶液 | D. | HNO3(HCl):使用AgNO3溶液 |
分析 A.氢氧化钡与硫酸钠反应生成硫酸钡沉淀和NaOH;
B.氢氧化钡与硫酸钾反应生成硫酸钡沉淀和KOH;
C.硝酸钡与硫酸钠反应生成硫酸钡沉淀和硝酸钠;
D.HCl与硝酸银反应生成氯化银沉淀和硝酸.
解答 解:A.氢氧化钡与硫酸钠反应生成硫酸钡沉淀和NaOH,则适量试剂可除杂,故A正确;
B.氢氧化钡与硫酸钾反应生成硫酸钡沉淀和KOH,则适量试剂可除杂,故B正确;
C.硝酸钡与硫酸钠反应生成硫酸钡沉淀和硝酸钠,引入新杂质硝酸钠,不能除杂,故C错误;
D.HCl与硝酸银反应生成氯化银沉淀和硝酸,则适量试剂可除杂,故D正确;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
2. 1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是MgO>CaO>NaCl>KCl,Na、Mg、Al第一电离能I1从小到大的排列顺序是Na、Al、Mg.
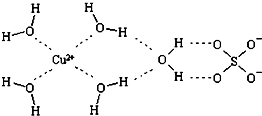
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示.
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是水分子间有氢键发生缔合作用.
②SO42-中S原子的杂化类型是sp3,与其互为等电子体的分子有CCl4(SiCl4)等(任写一种).
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有AC(填序号).
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式3d104s1;金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是$\frac{4M}{{N}_{A}(2\sqrt{2}r×1{0}^{-10})^{3}}$g/cm3(列出计算式).
 1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示.
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是水分子间有氢键发生缔合作用.
②SO42-中S原子的杂化类型是sp3,与其互为等电子体的分子有CCl4(SiCl4)等(任写一种).
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有AC(填序号).
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式3d104s1;金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是$\frac{4M}{{N}_{A}(2\sqrt{2}r×1{0}^{-10})^{3}}$g/cm3(列出计算式).
20.能够解释CO2比SiO2的熔、沸点低的原因是( )
| A. | CO2的相对分子质量比SiO2的相对分子质量小 | |
| B. | C-O键能小于Si-O键能 | |
| C. | C的原子半径小于Si | |
| D. | 破坏CO2晶体只需克服分子间作用力,破坏SiO2晶体要破坏Si-O共价键 |
7.能正确表示下列化学反的离子方程式是( )
| A. | 金属铝溶于盐酸中:Al+2H+═Al3++H2↑ | |
| B. | 碳酸镁溶于硝酸中:2H++CO32-═CO2↑+H2O | |
| C. | 在澄清的石灰水中通入少量的CO2:Ca2++2OH-+CO2═CaCO3↓+H2O | |
| D. | 饱和氯化铁溶液滴入沸水中:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ |
 如图为人体在某项生理过程中所发生的化学反应示意图.
如图为人体在某项生理过程中所发生的化学反应示意图.