题目内容
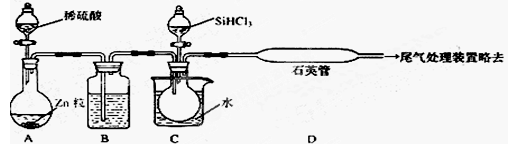
(14分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
试回答:
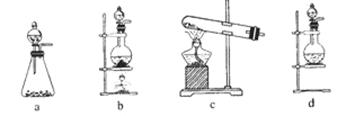
(1)该实验中A部分的装置是 (填写装置的序号)。
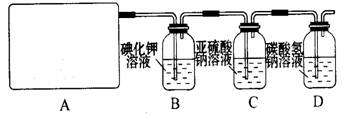
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:取漂白粉适量,研磨后溶解,配制成漂白液,运用下列实验,检测该漂白液的性质。
①将少量漂白液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测漂白液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向漂白液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。
请回答以下问题:
a、实验①表现出该消毒液具有 性;
b、实验②用pH试纸检测消毒液的操作是 _______________________;
c、实验③中涉及反应的离子方程式为 ____________;
 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
试回答:
(1)该实验中A部分的装置是 (填写装置的序号)。

(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):
。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式 。
(4)该实验存在明显的缺陷,请你提出改进的方法 。
(5)该小组又进行了如下实验:取漂白粉适量,研磨后溶解,配制成漂白液,运用下列实验,检测该漂白液的性质。
①将少量漂白液滴入含有淀粉的KI溶液中,溶液中出现蓝色;
②用pH试纸检测漂白液,试纸边缘为蓝紫色(pH=13),中间部分为白色;
③向漂白液中加入少量稀硫酸,溶液变为黄绿色,产生使湿润的淀粉KI试纸变蓝的气体。
请回答以下问题:
a、实验①表现出该消毒液具有 性;
b、实验②用pH试纸检测消毒液的操作是 _______________________;
c、实验③中涉及反应的离子方程式为 ____________;
(14分)
(1)b
(2)取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)Cl2+HCO3-=CO2+Cl-+HClO
(4)缺少尾气吸收装置
(5)a、氧化性;
b 、用干燥洁净的玻璃棒蘸取少量溶液,点在pH试纸上,并与标准比色卡对照读数;
c 、Cl-+ClO- +2H+=Cl2↑+H2O
(1)b
(2)取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)Cl2+HCO3-=CO2+Cl-+HClO
(4)缺少尾气吸收装置
(5)a、氧化性;
b 、用干燥洁净的玻璃棒蘸取少量溶液,点在pH试纸上,并与标准比色卡对照读数;
c 、Cl-+ClO- +2H+=Cl2↑+H2O
(1)实验室制氯气是固液加热装置,故选b
(2)Na2SO3被氧化为Na2SO4,故本题的目的是检验硫酸根离子的存在:取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)也就是生成了HClO:Cl2+HCO3-=CO2+Cl-+HClO
(4)氯气有毒,一定要有尾气处理装置
(5)①证明有碘单质的生成,说明消毒液具有氧化性;
②基本的实验操作;
③有氯气的生成:Cl-+ClO- +2H+=Cl2↑+H2O
(2)Na2SO3被氧化为Na2SO4,故本题的目的是检验硫酸根离子的存在:取C中溶液少量,加入稀盐酸和氯化钡溶液,看是否产生沉淀
(3)也就是生成了HClO:Cl2+HCO3-=CO2+Cl-+HClO
(4)氯气有毒,一定要有尾气处理装置
(5)①证明有碘单质的生成,说明消毒液具有氧化性;
②基本的实验操作;
③有氯气的生成:Cl-+ClO- +2H+=Cl2↑+H2O

练习册系列答案
相关题目