题目内容
【题目】用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( ) 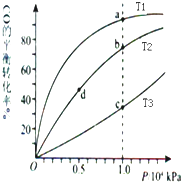
A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c) K(b)=K(d)
C.正反应速率:v(a)>v(c) v(b)>v(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
【答案】B
【解析】解:A.该反应为放热反应,温度越低,CO的转化率越大,则T1<T2<T3 , 故A错误;B.由图可知,a、c两点压强相同,平衡时a点CO转化率更高,该反应为放热反应,故温度T1<T3 , 降低温度平衡向正反应方向移动,则K(a)>K(c),平衡常数只与温度有关,b、d两点温度相同,平衡常数相同,则K(b)=K(d),故B正确;
C.由图可知,a、c两点压强相同,平衡时a点CO转化率更高,该反应为放热反应,温度越低,CO的转化率越大,故温度T1<T3 , 温度越高,反应速率越快,故υ(a)<υ(c).b、d两点温度相同,压强越大,反应速率越大,b点大于d点压强,则v(b)>v(d),故C错误;
D.CO转化率的越大,n总越小,由M= ![]() 可知,a点n总小,则M(a)>M(c),M(b)>M(d),故D错误;
可知,a点n总小,则M(a)>M(c),M(b)>M(d),故D错误;
故选B.

 口算能手系列答案
口算能手系列答案【题目】某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化. 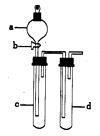
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是 .
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是 . 再由a向c中加2mL蒸馏水,c中的实验现象是 .
(3)如表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 , 理由是、 .
方 案 | 反 应 物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2 . 操作步骤为:实验现象为 .