题目内容
【题目】某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化. 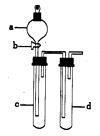
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是 .
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是 . 再由a向c中加2mL蒸馏水,c中的实验现象是 .
(3)如表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 , 理由是、 .
方 案 | 反 应 物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2 . 操作步骤为:实验现象为 .
【答案】
(1)检查装置气密性
(2)Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;反应变缓,红棕色气体逐渐变为无色
(3)丙;制取等量的硝酸铜时,丙方案耗酸量最少;无污染物(NOX)产生
(4)a中加入浓盐酸,c中加入高锰酸钾,d中加入溴化钾溶液 、 打开b由a向c中加入浓盐酸; c中有黄绿色气体产生,d中溶液由无色变为橙黄色 ;但此实验的不足之处是 无尾气处理装置,会污染环境
【解析】解:(1)实验前要检查装置气密性,实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,这是检查装置气密性的常见方法,
所以答案是:检查装置气密性;(2)铜与浓硝酸反应得到硝酸铜、二氧化氮和水,反应的化学方程式为:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;由a向c中加2mL蒸馏水,硝酸进行的稀释,反应变缓,同时二氧化氮能与水反应生成硝酸和一氧化氮,故c中气体颜色红棕色气体逐渐变为无色,
所以答案是:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;反应变缓,红棕色气体逐渐变为无色;(3)甲:铜与浓硝酸制取硝酸铜时的方程式是:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,生成的NO2会造成大气污染,硝酸的利用率为50%;
乙:铜与稀硝酸制取硝酸铜时的方程式是:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,生成的NO也会造成大气污染,硝酸的利用率为75%;
丙:此过程用方程式可表示为:2Cu+O2 ![]() 2CuO,CuO+2HNO3=Cu(NO3)2+H2O,从过程可以看出该过程不会产生有毒气体,环保且没有多消耗原料,故能体现绿色化学理念的最佳方案是丙,
2CuO,CuO+2HNO3=Cu(NO3)2+H2O,从过程可以看出该过程不会产生有毒气体,环保且没有多消耗原料,故能体现绿色化学理念的最佳方案是丙,
所以答案是:丙;制取等量的硝酸铜时,丙方案耗酸量最少;无污染物(NOX)产生;(4)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,利用KMnO4与浓盐酸反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,
再利用产生的氯气与KBr溶液反应得到溴:Cl2+2KBr=2KCl+Br2,操作步骤为a中加入浓盐酸,c中加入高锰酸钾,d中加入溴化钾溶液,打开b由a向c中加入浓盐酸,现象为c中有黄绿色气体产生,d中溶液变为橙色,同时要注意尾气吸收,防止污染空气,
所以答案是:a中加入浓盐酸,c中加入高锰酸钾,d中加入溴化钾溶液;打开b由a向c中加入浓盐酸;c中有黄绿色气体产生,d中溶液由无色变为橙黄色;无尾气处理装置,会污染环境.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案