题目内容
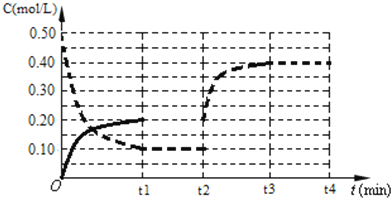
【题目】工业上通过反应“SiO2+2C![]() Si+2CO↑”制取单质硅,下列说法正确的是
Si+2CO↑”制取单质硅,下列说法正确的是
A. 自然界中硅元素均以SiO2形式存在
B. 高纯度晶体Si可用于制造光导纤维
C. 该反应条件下C的还原性比Si强
D. 标准状况下生成4.48 L CO时转移电子数为0.4×6.02×1023
【答案】D
【解析】工业上通过反应“SiO2+2C![]() Si+2CO↑”制取单质硅,下列说法正确的是
Si+2CO↑”制取单质硅,下列说法正确的是
A. 自然界中硅元素以硅酸盐和SiO2形式存在,A不正确;B. 高纯度晶体Si可用于电脑芯片等等,制造光导纤维用的是二氧化硅,B不正确;C. 此反应的发生不能说明该反应条件下C的还原性比Si强,因为该反应是一个熵增的反应,CO气体的生成对反应的发生起着重要作用,CO从反应体系中分离出来有利于化学平衡向正反应方向移动(与工业上用钠置换钾类似),所以C不正确;D. 该反应中电子转移的数目是4e-,标准状况下4.48 L CO的物质的量为0.2mol,所以转移电子数为0.4×6.02×1023,D正确,本题选D。

 全能测控一本好卷系列答案
全能测控一本好卷系列答案【题目】石油气“芳构化”是由石油气生产高辛烷值汽油的一种有效生产工艺。测得反应2C4H10![]() C8H10(g)+5H2在不同温度下的平衡常数变化如下:
C8H10(g)+5H2在不同温度下的平衡常数变化如下:
温度(℃) | 400 | 450 | 500 |
平衡常数K | a | 6a | 40a |
(1)该反应的正反应是________(填“吸热”或“放热”)反应。
(2)向2 L密闭定容容器中充入2 mol C4H10,反应10 s后测得H2浓度为1 mol·L-1,此10 s内,以C8H10表示的平均速率为____________________。
(3)能表示该反应在恒温恒容密闭容器中t1时刻后已经达平衡状态的图示是__________。

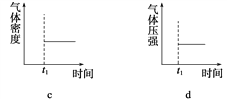
(4)下图表示某温度时将一定量的C4H10(含少量H2)充入容器中反应期间物质浓度随时间的变化(容器容积可变),实线代表C8H10,虚线代表C4H10。请用实线补充画出t1~t4间C8H10的浓度变化曲线。_____________