题目内容
14.1mol H2SO4中含1mol硫原子,2.408×1024个氧原子,50mol电子,一个硫酸分子的质量是1.63×10-22g.分析 1个H2SO4分子含有1个S原子、4个O原子、50个电子,硫原子物质的量等于硫酸的物质的量,氧原子物质的量为硫酸的4倍,电子物质的量为硫酸的50倍,根据N=nNA计算氧原子数目,根据$\frac{M}{{N}_{A}}$计算一个硫酸分子的质量.
解答 解:1个H2SO4分子含有1个S原子、4个O原子、50个电子,则:
n(S)=n(H2SO4)=1mol,
n(O)=4n(H2SO4)=4mol,故N(O)=4mol×6.02×1023mol-1=2.408×1024,
n(电子)=50n(H2SO4)=50mol,
一个硫酸分子的质量是$\frac{98g/mol}{6.02×1{0}^{23}mo{l}^{-1}}$=1.63×10-22g,
故答案为:1;2.408×1024;50;1.63×10-22.
点评 本题考查物质的量的有关计算,比较基础,注意掌握以物质的量为中心的有关计算.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
5.下列有关实验操作、现象或结论的叙述正确的是( )
| A. | 乙醇的催化氧化实验中铜丝主要起氧化剂的作用 | |
| B. | 用钠可以检验某无水酒精中是否含有水 | |
| C. | 制取乙烯时,温度计水银球置位于液面以下 | |
| D. | 除去甲烷中混有的少量乙烯,可以将混合气体通过酸性KMnO4溶液 |
2. 已知:2Fe2++Br2=2Fe3++2Br- 2Fe3++2I-=2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.则下列有关说法中正确的是( )
已知:2Fe2++Br2=2Fe3++2Br- 2Fe3++2I-=2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.则下列有关说法中正确的是( )
 已知:2Fe2++Br2=2Fe3++2Br- 2Fe3++2I-=2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.则下列有关说法中正确的是( )
已知:2Fe2++Br2=2Fe3++2Br- 2Fe3++2I-=2Fe2++I2.向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.则下列有关说法中正确的是( )| A. | 还原性:Fe2+>I->Br- | |
| B. | 当通入2molCl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | |
| C. | 原混合溶液中FeBr2的物质的量为6mol | |
| D. | 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
9.下列说法正确的是( )
| A. | 活化分子间所发生的碰撞为有效碰撞 | |
| B. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 | |
| C. | 升高温度能增加单位体积内活化分子的百分数和活化分子总数使反应速率增大 | |
| D. | 缩小容器的体积而增大压强,可增加活化分子总数,从而使反应速率增大 |
19.某同学按如图所示的装置进行试验.A、B为两种常见金属,它们的硫酸盐可溶于水.当K闭合时,在交换膜处SO42-从右向左移动.下列分析错误的是( )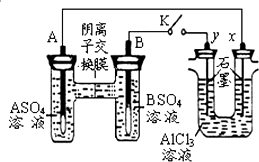

| A. | 金属活动性A强于B | |
| B. | 反应初期,y电极的电极反应为:2Cl--2e-=Cl2↑ | |
| C. | 反应初期,x电极周围出现白色沉淀,后来电极附近沉淀溶解 | |
| D. | 电解一段时间后将AlCl3溶液倒入烧杯并搅拌可得到偏铝酸盐溶液 |
6.下列变化过程中,同时有离子键、极性键、非极性键的断裂和形成的是( )
| A. | 2NH4HCO3=2NH3+CO2+2H2O | B. | 2NaOH+Cl2=NaCl+NaClO+H2O | ||
| C. | 2Na2O2+2CO2=2Na2CO3+O2 | D. | H2+Cl2=2HCl |
3.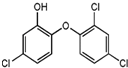 三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )
三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )
 三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )
三氯生的化学名为2,4,4-三氯-2-羟基二苯醚(如图),被广泛应用于肥皂、牙膏等日用化学品之中,有杀菌消毒等作用.则下列有关说法中不正确的是( )| A. | 该物质与浓溴水可发生取代反应 | |
| B. | 物质的分子式为C12H6Cl3O2 | |
| C. | 该物质中所有原子不一定在同一平面上 | |
| D. | 该物质苯环上的一溴取代物有6种 |
4.下列关于NH4Cl的说法中不正确的是( )
| A. | 氨气遇到HCl时,可以迅速反应生成NH4Cl | |
| B. | 0.5molNH4Cl中含有氢原子的质量是2克 | |
| C. | NH4Cl易溶于水,很稳定,受热不会分解 | |
| D. | 加热NH4Cl和碱的混合物,可以制取到氨气 |
 在如图所示的实验装置中,E为一张用淀粉碘化钾溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极.在A、B中充满AgNO3溶液后倒立于盛有AgNO3溶液的水槽中,再分别插入铂电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,B电极质量增重,A极产生无色气体.请回答下列问题:
在如图所示的实验装置中,E为一张用淀粉碘化钾溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极.在A、B中充满AgNO3溶液后倒立于盛有AgNO3溶液的水槽中,再分别插入铂电极.切断电源开关S1,闭合开关S2,通直流电一段时间后,B电极质量增重,A极产生无色气体.请回答下列问题: