题目内容
2.A和B两元素能形成AB2 型离子化合物,则A和B的原子序数可能是( )| A. | 6和8 | B. | 11和6 | C. | 20和8 | D. | 20和17 |
分析 活泼金属和活泼非金属之间易形成离子键,非金属元素之间易形成共价键(铵盐除外),含有离子键的化合物是离子化合物,AB2型离子化合物中A显+2价,B显-1价.
解答 解:A.6号元素是C元素,8号元素是O元素,这两种元素都是非金属元素,所以易形成共价化合物,故A错误;
B.11和6号元素分别为Na和C,C为-4价,不能形成AB2 型离子化合物,故B错误;
C.20号元素是Ca元素,8号元素是O元素,可生成CaO,故C错误;
D.20号元素是Ca元素,17号元素为Cl,可生成CaCl2,为离子化合物,故D正确.
故选D.
点评 本题考查了离子键、共价键的判断,难度不大,注意先根据元素符号判断元素,再根据化合价判断是否符合题意.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.X、Y、Z、W为四种短周期元素,它们的性质、原子结构等信息如表:
回答下列问题:
(1)W在元素周期表中的位置是第三周期第ⅦA 族.X、Y、W三种元素的简单离子半径大小是S2->Cl->Na+;(用离子符号表示)
(2)Y单质在氧气中燃烧的产物的电子式为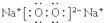 .用电子式表示元素X与Y形成化合物的过程
.用电子式表示元素X与Y形成化合物的过程 ;
;
(3)Z的气态氢化物的沸点反常,原因是NH3分子间存在氢键.元素W与元素X相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是②④;
①常温下W的单质和X的单质状态不同
②W的氢化物比X的氢化物稳定
③一定条件下W和X的单质都能与氢氧化钠溶液反应
④W的单质可以和X的氢化物水溶液反应置换出X
(4)Z2在一定条件下能和氢气反应生成气态氢化物,已知破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1molZ2中的化学键消耗的能量为Q2kJ,形成1molZ-H化学键释放的能量为O3kJ,则上述反应放出的能量可表示为6Q3-3Q1-Q2kJ.
| X | 原子M层上的电子数是原子核外电子层数的2倍 |
| Y | 短周期中原子半径最大的元素 |
| Z | 元素的单质为双原子分子,Z的氢化物水溶液呈碱性 |
| W | 元素最高正价是+7价 |
(1)W在元素周期表中的位置是第三周期第ⅦA 族.X、Y、W三种元素的简单离子半径大小是S2->Cl->Na+;(用离子符号表示)
(2)Y单质在氧气中燃烧的产物的电子式为
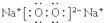 .用电子式表示元素X与Y形成化合物的过程
.用电子式表示元素X与Y形成化合物的过程 ;
;(3)Z的气态氢化物的沸点反常,原因是NH3分子间存在氢键.元素W与元素X相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是②④;
①常温下W的单质和X的单质状态不同
②W的氢化物比X的氢化物稳定
③一定条件下W和X的单质都能与氢氧化钠溶液反应
④W的单质可以和X的氢化物水溶液反应置换出X
(4)Z2在一定条件下能和氢气反应生成气态氢化物,已知破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1molZ2中的化学键消耗的能量为Q2kJ,形成1molZ-H化学键释放的能量为O3kJ,则上述反应放出的能量可表示为6Q3-3Q1-Q2kJ.
7.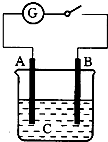 如图所示,把A、B插入C的溶液中,闭合电键后电流表的指针会发生偏转,且B上有气泡产生,则A、B、C可能是以下哪一组物质( )
如图所示,把A、B插入C的溶液中,闭合电键后电流表的指针会发生偏转,且B上有气泡产生,则A、B、C可能是以下哪一组物质( )
 如图所示,把A、B插入C的溶液中,闭合电键后电流表的指针会发生偏转,且B上有气泡产生,则A、B、C可能是以下哪一组物质( )
如图所示,把A、B插入C的溶液中,闭合电键后电流表的指针会发生偏转,且B上有气泡产生,则A、B、C可能是以下哪一组物质( )| A. | A-Cu B-Zn C-CuSO4 | B. | A-Ag B-Fe C-HCl | ||
| C. | A-Zn B-石墨 C-H2SO4 | D. | A-石墨 B-Zn C-H2SO4 |
14.将ag水煤气(成分为CO和H2)充分燃烧,将燃烧生成的气体(150℃)通过盛有过量的Na2O2的干燥管(反应气体无损失),充分反应后干燥管增重bg,则a和b的关系为( )
| A. | a=b | B. | a>b | C. | a<b | D. | 无法比较 |
12.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| B. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| C. | 向NaAlO2溶液中通入过量CO2:2 AlO+CO2+3H2O═2Al(OH)3↓+CO | |
| D. | 以下有机物在碱性条件下水解的化学方程式: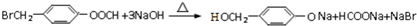 |
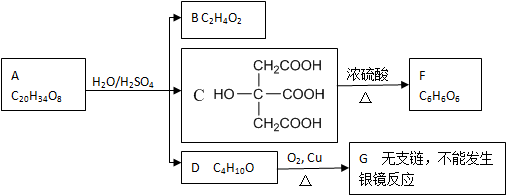
 .
. .
.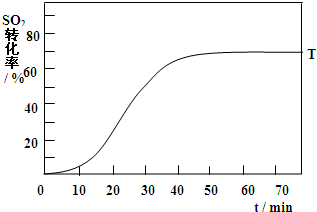 黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3.
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3.