题目内容
【题目】下列有关实验操作、现象和解释或结论都正确的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B | NO2球浸泡在冰水中 | 颜色变浅 | 生成N2O4的反应是吸热过程 |
C | Na2S2O3溶液与稀硫酸反应,改变反应的温度 | 只有浑浊产生,温度越高,出现浑浊时间越短 | 温度越高,反应速率越快 |
D | 向重铬酸钾稀溶液中滴加3-10滴浓硫酸 | 溶液橙色加深 | 加酸抑制Cr2O72-向CrO42-的转化 |
A.AB.BC.CD.D
【答案】D
【解析】
A.将过量的铁加入到稀硝酸中,发生反应:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O,产生Fe2+,充分反应后,滴入KSCN溶液,溶液不会变为红色,是硝酸先将Fe氧化为Fe3+,过量的铁再讲Fe3+还原为Fe2+,A错误;
B.NO2在密闭容器中存在化学平衡:2NO2(g)![]() N2O4(g),将NO2球浸泡在冰水中,颜色变浅,说明温度降低,平衡正向移动,根据平衡移动原理:降低温度,平衡向放热反应方向移动,生成N2O4的反应是放热过程,B错误;
N2O4(g),将NO2球浸泡在冰水中,颜色变浅,说明温度降低,平衡正向移动,根据平衡移动原理:降低温度,平衡向放热反应方向移动,生成N2O4的反应是放热过程,B错误;
C.Na2S2O3溶液与稀硫酸反应,Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,反应既有沉淀产生,也有气体放出,改变反应的温度,温度越高,出现浑浊时间越短,说明温度越高,反应速率越快,C错误;
D.重铬酸钾在溶液中存在平衡:Cr2O72-+H2O![]() 2CrO42- +2H+,向重铬酸钾稀溶液中滴加3-10滴浓硫酸,溶液的酸性增强,橙色加深,说明加酸平衡逆向移动,可以抑制Cr2O72-向CrO42-的转化,D正确;
2CrO42- +2H+,向重铬酸钾稀溶液中滴加3-10滴浓硫酸,溶液的酸性增强,橙色加深,说明加酸平衡逆向移动,可以抑制Cr2O72-向CrO42-的转化,D正确;
故选D。

【题目】![]() 和
和![]() 是两种重要的温室气体,通过
是两种重要的温室气体,通过![]() 和
和![]() 反应制造更高价值化学品是目前的研究目标。
反应制造更高价值化学品是目前的研究目标。
![]() 时,以镍合金为催化剂,向
时,以镍合金为催化剂,向![]() 容器中通入
容器中通入![]() 、
、![]() ,发生如下反应:
,发生如下反应:![]() 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:
物质 |
|
| CO |
|
体积分数 |
|
|
|
|
![]() 此温度下该反应的平衡常数
此温度下该反应的平衡常数![]() __________
__________
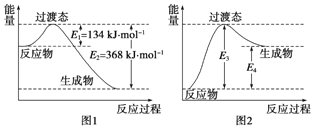
![]() 已知:
已知:![]()
![]()
![]()
![]()
![]()
反应![]() 的
的![]() _____________
_____________![]()
![]() 以二氧化钛表面覆盖
以二氧化钛表面覆盖![]() 为催化剂,可以将
为催化剂,可以将![]() 和
和![]() 直接转化成乙酸。
直接转化成乙酸。
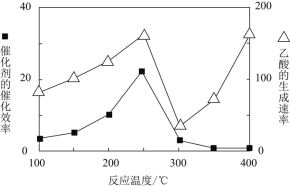
![]() 在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。![]() 时,温度升高而乙酸的生成速率降低的原因是___________。
时,温度升高而乙酸的生成速率降低的原因是___________。
![]() 为了提高该反应中
为了提高该反应中![]() 的转化率,可以采取的措施是_________。
的转化率,可以采取的措施是_________。
![]() 、
、![]() 、MgO均能吸收
、MgO均能吸收![]() ;
;
![]() 如果寻找吸收
如果寻找吸收![]() 的其他物质,下列建议不合理的是______
的其他物质,下列建议不合理的是______
![]() 可在具有强氧化性的物质中寻找
可在具有强氧化性的物质中寻找
![]() 可在碱性氧化物中寻找
可在碱性氧化物中寻找
![]() 可在ⅠA、ⅡA族元素形成的氧化物中寻找
可在ⅠA、ⅡA族元素形成的氧化物中寻找
![]() 吸收
吸收![]() 后,产物用于合成
后,产物用于合成![]() ,
,![]() 用于吸收、释放
用于吸收、释放![]() ,原理是:在
,原理是:在![]() ,
,![]() 与
与![]() 接触后生成
接触后生成![]() ;平衡后加热至
;平衡后加热至![]() ,反应逆向进行,放出
,反应逆向进行,放出![]() ,
,![]() 再生,说明该原理的化学方程式是_____________。
再生,说明该原理的化学方程式是_____________。
![]() 高温电解技术能高效实现下列反应:
高温电解技术能高效实现下列反应: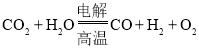 ,其可将释放的
,其可将释放的![]() 转化为具有工业利用价值的产品。工作原理示意图如下:
转化为具有工业利用价值的产品。工作原理示意图如下:
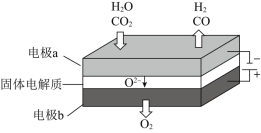
![]() 在电极a放电的电极反应式是____________。
在电极a放电的电极反应式是____________。