题目内容
【题目】有关下列化合物的说法不正确的是( )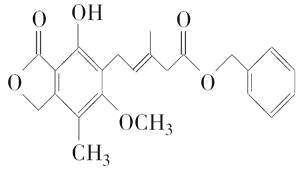
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
【答案】D
【解析】该有机物分子中含有碳碳双键,故可以与Br2发生加成反应,又含有甲基,故可以与Br2在光照下发生取代反应,A项正确;一个酚羟基可消耗一个NaOH,两个酯基可消耗两个NaOH,故B项正确;苯环可以催化加氢,碳碳双键可以使酸性KMnO4溶液褪色,故C项正确;该有机物中不存在羧基,故不能与NaHCO3溶液反应放出CO2气体,D项错误。

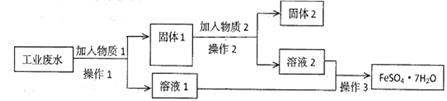
【题目】Ⅰ.制备水杨酸对正辛基苯基酯( ![]() )的过程如下:
)的过程如下:
步骤一:将水杨酸晶体投入到三颈烧瓶中,再加入适量的氯苯作溶剂并充分搅拌使晶体完全溶解,最后加入少量的无水三氯化铝。
步骤二:按下图所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2 , 反应制得水杨酰氯。
该反应方程式为: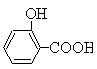 (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ 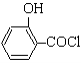 (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑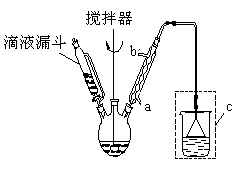
步骤三:将三颈烧瓶中混合液升温至80℃,再加入对正辛苯酚[ ![]() ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥即得产品。
(1)实验时,冷凝管中的冷却水进口为 (选填“a”或“b”);
(2)步骤一中加入无水三氯化铝的作用是 。
(3)步骤三中发生反应的化学方程式为 。
(4)Ⅱ.PCl3可用于半导体生产的外延、扩散工序。有关物质的部分性质如下:
熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其他 | |
白磷 | 44.1 | 280.5 | 1.82 | 2P(过量)+3Cl2 |
PCl3 | -112 | 75.5 | 1.574 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
POCl3 | 2 | 105.3 | 1.675 | 遇水生成H3PO4和HCl,能溶于PCl3 |
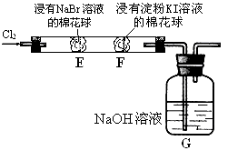
已知下图是实验室制备PCl3的装置(部分仪器已省略),则: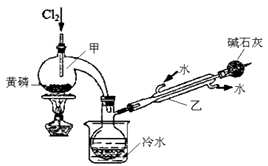
实验室制备Cl2的离子反应方程式为:。
(5)碱石灰的作用除了防止空气中的O2和水蒸气进入并与产品发生反应外还有:。
(6)向仪器甲中通入干燥Cl2之前,应先通入一段时间的干燥CO2 , 其目的是。
(7)测定产品中PCl3纯度的方法如下:迅速称取m g产品,水解完全后配成500mL溶液,取出25.00mL加入过量的c1 mol/L V1 mL 碘溶液,充分反应后再用c2 mol/L Na2S2O3溶液滴定过量的碘,终点时消耗V2 mL Na2S2O3溶液。已知:H3PO3+H2O+I2=H3PO4+2HI;I2+2Na2S2O3=2NaI+Na2S4O6;假设测定过程中没有其他反应,则根据上述数据,求出该产品中PCl3的质量分数为 (用含字母的代数式表示、可不化简)。
【题目】化学与生产生活密切相关,下列物质的用途及解释均正确的是
选项 | 用途 | 解释 |
A | 可用FeCl3溶液刻蚀铜制电路板 | Fe3+的氧化性强于Cu2+ |
B | 碳与石英反应可冶炼粗硅 | 碳的非金属性比硅强 |
C | 四氯化碳可用于灭火 | 四氯化碳的沸点高 |
D | 酸性KMnO4溶 液可漂白织物 | KMnO4有强氧化性 |
A. A B. B C. C D. D