题目内容
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。
(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/mol
S(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol
一定条件下,可以通过CO与SO2反应生成S(1)和一种无毒的气体,实现燃煤烟气中硫的回收,写出该反应的热化学方程式_______________________________。
(2)一定温度下,向2L恒容密闭容器中通入2molCO和1molSO2,发生上述(1)中回收硫的反应。若反应进行到20min时达平衡,测得CO2的体积分数为0.5,则前20min的反应速率ν(CO)= _________,该温度下反应化学平衡常数K=____________(L·mol-1)
(3)在不同条件下,向2L恒容密闭容器中通入2molCO和1molSO2,反应体系总压强随时间的变化如图(Ⅰ)所示:
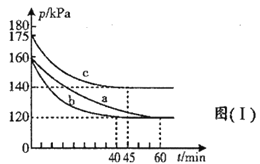
①图(Ⅰ)中三组实验从反应开始至达到平衡时,v(CO)最大的为___________(填序号)
②与实验a相比,c组改变的实验条件可能是_________________。
(4)“亚硫酸盐法”吸收烟气中的SO2。室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图(Ⅱ)所示,b点时溶液pH=7,则n(NH4+)∶n(HSO3-)=______。

(5)间接电化学法可除NO。其原理如图(Ⅲ)所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)_______________________________。

【答案】 2CO(g)+SO2(g)=S(l)+2CO2(g) ΔH=-270kJ/mol 0.03mol·L-1·min-1 11.25 b 升高温度 3:1 2HSO3-+2e-+12H+=S2O42-+6H2O
【解析】(1)已知:2CO(g)+O2(g)=2CO2(g) ΔH1=-566kJ/mol;S(l)+O2(g)=SO2(g) ΔH2=-296kJ/mol;根据盖斯定律:第一个反应减去第二个反应得:2CO(g)+SO2(g)=S(l)+2CO2(g) ΔH=-270kJ/mol;正确答案:2CO(g)+SO2(g)=S(l)+2CO2(g) ΔH=-270kJ/mol。
(2)设参加反应的SO2的物质的量为![]() ,则有
,则有
![]()
初始状态![]()
![]()
反应的量![]()
![]()
![]()
![]()
平衡状态![]()
![]()
![]()
![]()
即:![]() ,
,![]() ,ν(CO)=(0.6×2)/(2×20)=0.03mol·L-1·min-1 ;c(CO)=(2-1.2)/2=0.4mol/L, c(SO2)=(1-0.6)/2=0.2 mol/L, c(CO2)=1.2/2=0.6 mol/L, 该温度下反应化学平衡常数K=c2(CO2)/c2(CO)×c(SO2)= 0.62/0.42×0.2=11.25(L·mol-1);正确答案:0.03mol·L-1·min-1; 11.25。
,ν(CO)=(0.6×2)/(2×20)=0.03mol·L-1·min-1 ;c(CO)=(2-1.2)/2=0.4mol/L, c(SO2)=(1-0.6)/2=0.2 mol/L, c(CO2)=1.2/2=0.6 mol/L, 该温度下反应化学平衡常数K=c2(CO2)/c2(CO)×c(SO2)= 0.62/0.42×0.2=11.25(L·mol-1);正确答案:0.03mol·L-1·min-1; 11.25。
(3)根据图示,达到平衡的时间快慢为:![]() ,因此达到平衡时的反应速率v(CO)大小为
,因此达到平衡时的反应速率v(CO)大小为![]() ,因此v(CO)最大的为b;正确答案:b。
,因此v(CO)最大的为b;正确答案:b。
②与实验a相比,c组反应前和反应后的压强均变大,且达到平衡时间减少,因此改变的实验条件可能是升高温度;正确答案: 升高温度。
(4)A点时,n(HSO3-):n(H2SO3)=1:1,b点时溶液的pH=7,根据电荷守恒:n(NH4+)= n(HSO3-)+2n(SO32-),又根据图可知:n(HSO3-)= n(SO32-),n(NH4+):n(HSO3-)=(1+2):1=3:1;正确答案:3:1。
(5)根据图示可知,阴极发生还原反应:HSO3- 变为S2O42-,电极反应式为2HSO3-+2e-+12H+=S2O42-+6H2O;正确答案:2HSO3-+2e-+12H+=S2O42-+6H2O。