题目内容
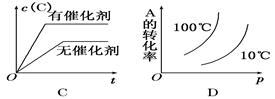
如图所示的各图中,表示2A(g)+B(g)  2C(g)(正反应放热)这个可逆反应的正确图像为
2C(g)(正反应放热)这个可逆反应的正确图像为

 2C(g)(正反应放热)这个可逆反应的正确图像为
2C(g)(正反应放热)这个可逆反应的正确图像为

A
正反应是放热反应,所以升高温度,反应速率加快,平衡向逆反应方向进行,反应物的转化率降低,生成物的含量降低,A正确,D不正确;增大压强,正逆反应速率都是增大的,B不正确;催化剂不能改变平衡状态,C不正确,答案选A。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
题目内容
 2C(g)(正反应放热)这个可逆反应的正确图像为
2C(g)(正反应放热)这个可逆反应的正确图像为


 备战中考寒假系列答案
备战中考寒假系列答案