��Ŀ����
����Ŀ��̼��﮹㷺Ӧ�����մɺ�ҽҩ��������﮻�ʯ����Ҫ�ɷ�ΪLiAlSi2O6��Ϊԭ�����Ʊ�Li2CO3�Ĺ����������£�
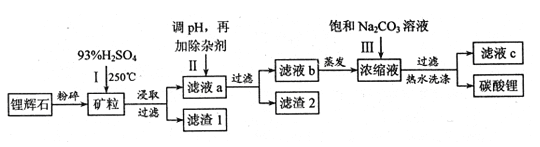
��֪��2LiAlSi2O6+H2SO4![]() Li2SO4+Al2O34SiO2H2O
Li2SO4+Al2O34SiO2H2O
��Fe3+��Al3+��Fe2+��Mg2+������������ʽ��ȫ����ʱ����Һ��pH�ֱ�Ϊ3.2��4.7��9.0��11.1
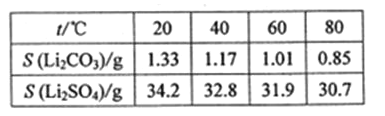
��ijЩ���ʵ��ܽ����S�����±�
��ش��������⣺
��1��﮻�ʯ��Ũ�����ȡ֮ǰҪ�����ϸ������Ŀ���� ��
��2����Һa�к���Li+��SO42-��������Fe3+��Al3+��Fe2+�� Mg2+ ��Ca2+ ��Na+�����ʣ����������ڽ����¼���ʯ��ʯ�Ե�����Һ��pH��6.0��6.5����ʱ���������������� ��ʯ��ʯ������ҺpH��ԭ�������ӷ���ʽΪ ��
��3������������Һa�м���ij��Ӽ�����Ϊ������H2O2��Һ��ʯ�����Na2CO3��Һ������������ԭ��Ӧ�����ӷ���ʽΪ ��
��4���������м��뱥��Na2CO3��Һ���˺���Ҫ����ˮϴ�ӵ�ԭ���� ��
��5������Һc�пɻ��յ���Ҫ������ ��
���𰸡���1������﮻�ʯ������ĽӴ�������ӿ������Ӧ��������߽�������2����
��2��Al3+��Fe3+��1������CaCO3+2H+=Ca2++H2O+CO2����2����
��3��2Fe2+��H2O2��2H+=2Fe3+��2H2O����2����
��4��Li2CO3���ܽ�����¶����߶���С����ˮϴ�ӿɼ���Li2CO3����ʧ��2������5��Na2SO4��1����
��������
�����������1��﮻�ʯ��Ũ�����ȡ֮ǰҪ�����ϸ������������������ĽӴ�������ӿ������Ӧ��������߽����ʡ�
��2���ڽ����¼���ʯ��ʯ�Ե�����Һ��pH��6.0��6.5����ʱ��ΪFe3+��Al3+��ȫ�γ������������ʱ����Һ��pH�ֱ�Ϊ3.2��4.7��������pHֵ������ 6.0��6.5���ʴ�ʱ����������������Al3+��Fe3+ ��ʯ��ʯ������ҺpH��ԭ�������ӷ���ʽΪCaCO3+2H+=Ca2++H2O+CO2����
��3������˫��ˮ�ܰ��������������������ӣ���Ӧ�����ӷ���ʽΪ��2Fe2+��H2O2��2H+=2Fe3+��2H2O�������ķ�Ӧ���Ǹ��ֽⷴӦ��
��4�����ݱ�����̼��﮵��ܽ�����¶ȵĹ�ϵ��֪��Li2CO3���ܽ�����¶����߶���С����ˮϴ�ӿɼ���Li2CO3����ʧ��
��5���������Ƿ����˸��ֽⷴӦ����������Һc�пɻ��յ���Ҫ������Na2SO4��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�